Zilver
Inhoudsopgave
Zilver speelt vaak de tweede viool na een ander edelmetaal, goud. Maar dit element heeft bijzondere eigenschappen die een goede uitstraling verdienen.
Van alle metalen is zuiver zilver bijvoorbeeld de beste geleider van warmte en elektriciteit. Het is ook de beste reflector van zichtbaar licht en daarom wordt het vaak gebruikt om spiegels van te maken, hoewel zilver verkleurt en donkergrijs wordt wanneer wordt blootgesteld aan lucht en daarom regelmatig moet worden gepoetst.
Zuiver zilver is te zacht voor producten als sieraden en tafelgerei dus de beste vorken en messen van de familie zijn hoogst waarschijnlijk gemaakt van zogenaamd sterling zilver. Dit is een legering van 92,5% zilver en 7,5% koper (hoewel soms ook andere metalen worden gebruikt). Zilver wordt ook gebruikt in elektronica en batterijen. Omdat het metaal antimicrobiële eigenschappen heeft kunnen nanodeeltjes zilver in kleding worden verwerkt om zo te voorkomen dat bacteriën zich ophopen op afzettingen van zweet en olie.
Chemische gegevens
| Symbool | Ag |
| Volledige naam | Zilver |
| Atoomnummer | 47 |
| Atoommassa (g.mol-1 ) | 107,8682 |
| Groep | transitiemetalen |
| Elektronegativiteit (Pauling) | 1,93 |
| Dichtheid (g.cm-3 bij 20 °C) | 10,501 |
| Smeltpunt (°C) | 961,78 |
| Kookpunt (°C) | 2162 |
| Vanderwaalsstraal (nm) | 0,172 |
| Ionstraal | 0,126 |
| Isotopen | 2 stabiel |
| Elektronenschil | [Kr]4d105s2 |
| Elektronen per schil | 2, 8, 18,18,1 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 731,0 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 2070 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 3361 |
| Standaardpotentiaal (V) | — |
| Ontdekt door: | vóór 5000 v. Christus |
Bohr – Rutherford diagram
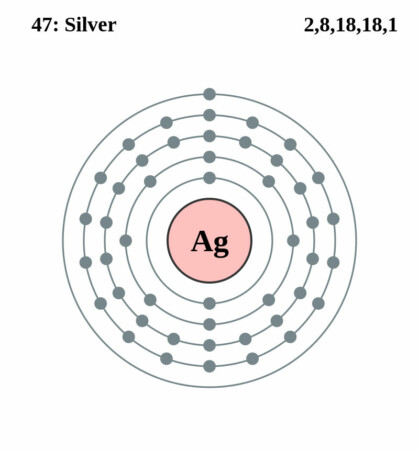
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 47 | Zilver | 107 Ag | 106,905093 | 51,839 |
| 109 Ag | 108,904756 | 48,161 |
Radioisotopen
|
Nuclide |
Isotopische massa (u) |
Halfwaardetijd |
|---|---|---|
|
93Ag |
92,94978 |
5 ms |
|
94Ag |
93,94278 |
37 ms |
|
95Ag |
94,93548 |
1,74 s |
|
96Ag |
95,93068 |
4,45 s |
|
97Ag |
96,92397 |
25,3 s |
|
98Ag |
97,92157 |
47,5 s |
|
99Ag |
98,91760 |
124 s |
|
100Ag |
99,91610 |
2,01 min |
|
101Ag |
100,9128 |
11,1 min |
|
102Ag |
101,9116 |
12,9 min |
|
103Ag |
102,9089 |
65,7 min |
|
104Ag |
103,9086 |
69,2 min |
|
105Ag |
104,9065 |
41,29 dagen |
|
106Ag |
105,9066 |
23,96 min |
|
108Ag |
107,9059 |
2,37 min |
|
110Ag |
109,9061 |
24,6 s |
|
111Ag |
110,9052 |
7,45 dagen |
|
112Ag |
111,9070 |
3,130 uur |
|
113Ag |
112,9065 |
5,37 uur |
|
114Ag |
113,9088 |
4,6 s |
|
115Ag |
114,9087 |
20,0 min |
|
116Ag |
115,9113 |
2,68 min |
|
117Ag |
116,9116 |
73,6 s |
|
118Ag |
117,9145 |
3,76 s |
|
119Ag |
118,9156 |
6,0 s |
|
120Ag |
119,9187 |
1,23 s |
|
121Ag |
120,9198 |
0,79 s |
|
122Ag |
121,9235 |
0,529 s |
|
123Ag |
122,9249 |
0,300 s |
|
124Ag |
123,9286 |
172 ms |
|
125Ag |
124,9304 |
166 ms |
|
126Ag |
125,9345 |
107 ms |
|
127Ag |
126,9367 |
79 ms |
|
128Ag |
127,9411 |
58 ms |
|
129Ag |
128,9436 |
44 ms |
|
130Ag |
129,9504 |
± 50 ms |
Geschiedenis van zilver
Zilver heeft al een lange geschiedenis. Het oudste bewijs dat er zilver werd gewonnen gaat terug tot ongeveer 3000 jaar voor Christus toen er in het tegenwoordige Turkije en Griekenland al zilver werd gebruikt. De mensen in de oudheid wisten zelfs al hoe ze zilver moesten zuiveren. Ze verhitten zilvererts en bliezen er hete lucht over. Het zilver reageert niet met de lucht maar de andere metalen in het erts zoals koper en lood oxideren en kunnen op deze manier van het edelmetaal worden gescheiden. Dit proces wordt cupellatie genoemd.
Zilver, maar ook goud, ontstaat tijdens explosies van zware sterren, de zogenaamde supernova-explosies.
Op Aarde explodeerde zilver pas goed toen de Europeanen in 1492 Amerika ontdekten. Spaanse veroveraard ontdekten dat Zuid-Amerika rijk aan zilver en goud was en dat werd in grote aantallen naar Europa toe gehaald. Tussen 1500 en 1800 was ongeveer 85% van het wereldwijd geproduceerde zilver afkomstig uit Bolivia, Peru en Mexico.
Zilver speelde een belangrijke rol bij het mogelijk maken van de vroege fotografie. Zilvernitraat (AgNO3) werd gebruikt in de eerste generatie fotografische platen. Het reageert met licht en wordt dan zwart waardoor fotografen een moment van licht vast kunnen leggen. Zelfs met de opkomst van digitale camera’s blijft zilver onderdeel van het traditionele fotografieproces. Vanaf 2003 wordt nog steeds ongeveer 1900 ton zilver gebruikt voor fotografische doeleinden. Ongeveer 1200 ton wordt jaarlijks gebruikt in de elektronica-industrie. Voor sieraden etc. wordt ongeveer 500 ton per jaar gebruikt en ongeveer 1800 ton gaat jaarlijks naar verschillende andere toepassingen.
Weetjes
Het atoomsymbool van zilver is Ag en dat is misschien en beetje vreemd in relatie tot de naam van het element. Ag stamt af van argentum en dat is het Latijnse woord voor zilver.
Mensen vinden zilver mooi. Archeologen hebben op een 3200 jaar oude locatie in Israël al zilveren sieraden gevonden.
Zilver heeft anti-microbiologische eigenschappen maar dat maakt het nog geen geschikt middel voor thuisgebruik. In de homeopathie wordt soms colloïdaal zilver gebruikt voor een scala aan gezondheidsklachten maar het drinken van hoge concentraties zilver leidt tot een blauwe huid.
Laat je goede tafelzilver een jaar lang in een lade liggen en het zal waarschijnlijk zijn verkleurd. Hoe blijven dan de zilverstukken in een museum zo mooi glanzend? Die worden bedekt met transparante lakken. Onderzoekers werken aan coatings van enkele nanometer dik die de huidige handgeschilderde lakken kunnen vervangen door iets dunners dat volledig onzichtbaar en veel duurzamer is.
Huidig onderzoek
De anti-microbiologische eigenschappen van zilver hebben het element ook in de trukendoos van artsen gebracht. Zilver wordt al honderden jaren gebruikt om infecties van wonden te voorkomen. Zilver doodt in zijn elementaire vorm geen bacteriën. Het metaal werkt alleen in ionvorm, het moet een elektron verliezen om positief geladen te worden. Het positief geladen zilverion interfereert met de celwanden van bacteriën en verstoort andere microbiële processen.
Patiënten met brandwonden kunnen op zilver gebaseerde crèmes op hun verwondingen gebruiken en sommige ziekenhuizen gebruiken met zilver doordrenkte verbanden voor huidzweren en andere vormen van wondverzorging. Er zijn echter discussies over de werkzaamheid van deze verbanden.
Sommige fabrikanten hebben de anti-microbiologische magie van zilver aangegrepen als een marketingkans door zilver in textiel te verwerken en dan te beweren dat het vervelende transpiratiegeuren, veroorzaakt door bacteriën, voorkomt.
Onderzoek heeft echter aangetoond dat het zilver zelden in de gewenste vorm aanwezig is waardoor dergelijke claims eigenlijk nergens op berusten.