Neerslagtitraties – het verschil tussen Mohr en Volhard
Inhoudsopgave
Het belangrijkste verschil tussen de Mohr- en Volhardmethode is dat bij de Mohr-methode zilverionen reageren met halogenide-ionen in aanwezigheid van een chromaatindicator, terwijl bij de Volhard-methode een overmaat aan zilverionen reageert met halogenide-ionen.
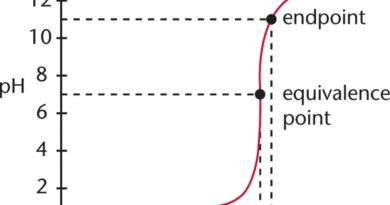
Titrimetrie is een volumetrische analyse die wordt gebruikt om de hoeveelheid analyt in een monsteroplossing te bepalen. Hierbij wordt een titrant in de buret gevuld, een pipet gebruikt om de analyt in de erlenmeyer te brengen waar de reactie plaatsvindt. De titrant met een bekende concentratie wordt toegevoegd totdat de reactie is voltooid (chemisch equivalentiepunt). Het eindpunt van de titratie is het punt waarop de reactie is voltooid.
Om het eindpunt te detecteren wordt een indicator gebruikt die op het eindpunt van kleur verandert. Als alternatief wordt ook een instrumentele methode gebruikt zoals een pH-meter, potentiometer of geleidbaarheidsmeter. Er zijn vier soorten titraties, gebaseerd op de chemische reactie tussen de titrant en de opgeloste stof, zoals zuur-basetitratie, redoxtitratie, complexometrische titratie en neerslag(precipitatie)titratie.
Wat is een neerslagtitratie?
Een neerslagtitratie is een type titratie waarbij sprake is van de vorming van een neerslag tijdens het titratieproces. Een neerslagtitratie verwijst naar de volumetrische methode die afhankelijk is van de vorming van een licht oplosbaar neerslag, terwijl argentometrie verwijst naar neerslagtitraties met zilvernitraat (AgNO3) als neerslagmiddel.
Het principe van een neerslagtitratie is dat de hoeveelheid toegevoegd precipitaat = de hoeveelheid geprecipiteerde analyt. De titrant reageert met een verbinding en vormt een onoplosbare stof die neerslag wordt genoemd. Dit gaat door totdat alle verbindingen zijn verbruikt, waarbij zilverionen worden gebruikt om het chloridegehalte te bepalen.
De Mohr-, Volhard– en Fajan-methode zijn belangrijke analysetechnieken om de concentratie van halogeniden en bepaalde metaalionen te bepalen. Deze methodes zijn genoemd naar de wetenschappers die deze methodes hebben ontwikkeld.
Wat is de Mohr-methode?
De Mohr-methode is een soort neerslagtitratie die voor het eerst werd beschreven door de Duitse chemicus Karl Friedrich Mohr. Het is een directe titratiemethode om de chloriden te bepalen door middel van titratie met zilvernitraat.
De methode gebruikt de chromaationen (CrO42-) als indicator voor de argentometrische bepaling van bromide, cyanide- en chloride-ionen.
De Mohr-methode is effectiever in het pH-gebied tussen 6 en 9; boven die pH0gebied slaat zilver neer met het hydroxide. Wanneer alle chloride-ionen door het zilverion zijn verbruikt, ontstaat een roodbruin gekleurd neerslag als gevolg van de reactie tussen het zilverion en het chromaation.
Wat is de Volhard-methode?
De Volhard-methode is een soort neerslagtitratie en een voorbeeld van een terugtitratie, voor het eerst beschreven door de Duitse chemicus Jacob Volhard in 1874. De methode wordt gebruikt om de halogenideconcentratie te bepalen met behulp van een terugtitratie, waarbij een chlorideoplossing wordt getitreerd met zilverionen en vervolgens het overschot aan zilverionen in het monster wordt bepaald.
De indicator in dit experiment is een oplossing met ijzerionen, die met thiocyanaationen een rode kleur kan produceren. Een thiocyanaat-ionenoplossing wordt gebruikt om het teveel aan zilverionen te titreren. In dit geval reageert het thiocyanaat met zilverionen in plaats van met ijzerionen. Het thiocyanaat daarentegen zal reageren met ijzerionen nadat alle zilverionen zijn gebruikt. Omdat ijzerionen ijzerhydroxide vormen in aanwezigheid van een basisch medium, met de oplossing zuur blijven.
Verschil tussen de Mohr- en de Volhard-methode
- Bij de titratie van Mohr wordt zilvernitraat gebruikt als titrant en chloride-ionenoplossing als analyt, terwijl bij de Volhard-methode een overmaat zilvernitraat wordt gebruikt om chloriden neer te slaan, die vervolgens worden getitreerd met kalium- of natriumthiocyanaat.
- De Mohr-methode is een directe titratie, terwijl de Volhard-methode een indirecte titratiemethode is.
- Bij de titratie volgens Mohr wordt aan het eindpunt een gekleurd neerslag gevormd, terwijl de titratie volgens Volhard aan het eindpunt een oplosbaar, gekleurd complex wordt gevormd.
- Bij de Mohr-methode wordt kaliumchromaat gebruikt als indicator terwijl bij Volhard ijzerammoniumsulfaat als indicator wordt gebruikt.
- De Mohrmethode vereist neutrale of alkalische omstandigheden terwijl de Volhard-methode zure omstandigheden vereist.
- De Mohr-titratie wordt uitgevoerd bij kamertemperatuur, terwijl de Volhard-methode wordt uitgevoerd bij temperaturen onder 20 °C.
- Jodium en cyanaat kunnen niet worden getitreerd met de Mohr-methode terwijl jodide, bromide en chloride kunnen worden bepaald volgens de Volhard-methode.
Eerste publicatie: 1 april 2023