Yttrium
Inhoudsopgave
Yttrium werd aan het einde van de 18de eeuw ontdekt maar pas sinds de laatste tientallen jaren wordt dit zachte zilverkleurige metaal algemeen gebruikt. Er zijn toepassingen in de chemie, natuurkunde, computertechnologie, energie, medicijnen en nog veel meer gebieden.
In het periodieke systeem der elementen behoort yttrium tot de transitiemetalen. Tot deze groep behoren ook de veel bekendere elementen ijzer en zilver. Transitiemetalen zijn sterk maar buigzaam en die eigenschappen zorgen ervoor dat elementen als koper en nikkel voor in bedradingen worden gebruikt. Draden en staven van yttrium worden ook gebruikt in elektronica en zonne-energie. Yttrium wordt ook gebruikt in lasers, keramiek, cameralenzen en tientallen andere producten.
Yttrium is ook een van de zeldzame aardmetalen. Ondanks hun naam komen de meeste zeldzame aardmetalen in grote hoeveelheden op Aarde voor. De 17 zeldzame aardmetalen bevatten o.a. yttrium, scandium en de 15 lanthaniden (de metallische elementen met de atoomnummers 57 tot 71). Deze elementen zijn onmisbaar geworden bij de productie van mobiele telefoons en andere technologie.
Yttrium wordt echter zelden alleen gebruikt. Het wordt meestal in verbindingen gebruikt zoals yttrium barium koperoxide. Deze verbinding wordt toegepast in het onderzoek naar hoge temperatuur supergeleidbaarheid. Yttrium wordt ook toegevoegd aan metaallegeringen omdat het corrosie en oxidatie tegengaat.
Yttrium en zijn verbindingen worden vaak toegevoegd aan andere materialen om zo de eigenschappen van die andere materialen te verbeteren.
Chemische gegevens
| Symbool | Y |
| Volledige naam | Yttrium |
| Atoomnummer | 39 |
| Atoommassa (g.mol-1 ) | 88,906 |
| Groep | Transitiemetalen |
| Elektronegativiteit (Pauling) | 1,22 |
| Dichtheid (g.cm-3 bij 20 °C) | 4,472 |
| Smeltpunt (°C) | 1526 |
| Kookpunt (°C) | 2930 |
| Vanderwaalstraal (nm) | 0,160 (+3) |
| Ionstraal (nm) | — |
| Isotopen | 1 stabiel |
| Elektronenconfiguratie | [Kr]4d15s2 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 600 |
| Tweede ionisatie potentiaal (kJ.mol-1 ) | 1180 |
| Derder ionisatiepotentiaal (kJ.mol-1 ) | 1980 |
| Standaard potentiaal (V) | — |
| Ontdekt door | Johan Gadolin in 1794 |
Geschiedenis
In 1787 ontdekte de Zweedse luitenant en partime chemicus Carl Axel Arrhenius in de buurt van Ytterby een ongewoon zwart stuk gesteente. Ytterby is een kleine stad in de buurt van de Zweedse hoofdstad Stockholm. Hij dacht dat hij een nieuw mineraal gehad gevonden dat wolfraam bevatte. Hij stuurde het ter analyse naar de Finse Mineraloog en chemicus Johan Gadolin.
Gadolin isoleerde het yttrium in het mineraal. Dit mineraal werd later naar hem vernoemd: Gadoliniet. Yttrium is vernoemd naar de vindplaats Ytterby.
In 1843 bestudeerde de Zweedse chemicus Carl Gustaf Mosander samples van yttrium en hij ontdekte drie oxides. In die tijd werden ze yttria, erbia en terbia genoemd. Nu zijn ze bekend als het witte yttriumoxide, het gele terbiumoxide en het roze erbiumoxide. In 1878 werd een vierde oxide gevonden. Dit was ytterbiumoxide.
Bohr-Rutherford diagram
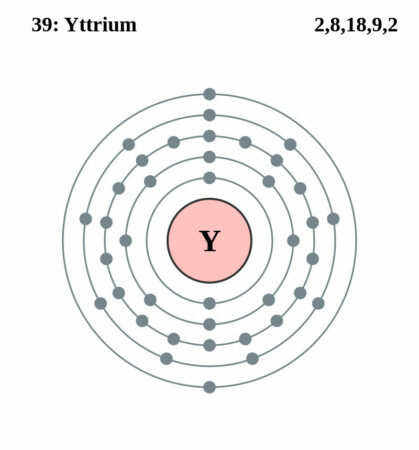
Isotopen
| Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|
| Yttrium | 89 Y | 88,905848 | 100 |
Radioisotopen
| Nuclide | Isotopische massa (u) | Halveringstijd |
|---|---|---|
| 76Y | 75,95845 | 500 ns |
| 77Y | 76,94965 | 63 ms |
| 78Y | 77,94361 | 54 ms |
| 79Y | 78,93735 | 14,8 s |
| 80Y | 79,93428 | 30,1 s |
| 81Y | 80,92913 | 70,4 s |
| 82Y | 81,92679 | 8,30 s |
| 83Y | 82,92235 | 7,08 min |
| 84Y | 83,92039 | 4,6 s |
| 85Y | 84,91643 | 2,68 uur |
| 86Y | 85,91488 | 14,74 uur |
| 87Y | 86,91087 | 79,8 uur |
| 88Y | 87,90950 | 106,616 dagen |
| 90Y | 89,90715 | 64,053 uur |
| 91Y | 90,90730 | 58,51 dagen |
| 92Y | 91,90894 | 3,54 uur |
| 93Y | 92,90958 | 10,18 uur |
| 94Y | 93,91159 | 18,7 min |
| 95Y | 94,91282 | 10,3 min |
| 96Y | 95,91589 | 5,34 s |
| 97Y | 96,91813 | 3,75 s |
| 98Y | 97,92220 | 0,548 s |
| 99Y | 98,92463 | 1,470 s |
| 100Y | 99,92776 | 735 ms |
| 101Y | 100,9303 | 426 ms |
| 102Y | 101,9335 | 0,30 s |
| 103Y | 102,9367 | 224 ms |
| 104Y | 103,9410 | 180 ms |
| 105Y | 104,9448 | 60 ms |
| 106Y | 105,9497 | 50 ms |
| 107Y | 106,9541 | 30 ms |
| 108Y | 107,9594 | 20 ms |
Bronnen van yttrium
Ofschoon yttrium in Scandinavië is ontdekt komt het in andere landen veel meer voor. China Rusland, India, Maleisië en Australië zijn de grootste producenten van yttrium. In april 2018 werd op het Japanse eiland Minamitori een grote vindplaats van zeldzame aardmetalen, waaronder yttrium, gevonden.
Yttrium komt voor in de meeste zeldzame aardemineralen maar het is nooit als vrij element in de korst van de Aarde aangetroffen. Maangesteente dat de Apollo’s naar de Aarde hebben gebracht bevat ook yttrium. Ook in ons eigen lichamen komen kleine hoeveelheden yttrium voor, voornamelijk in de lever de nieren en de botten.
Toepassingen van yttrium
Voor de opkomst van de flatscreen televisies hadden televisietoestellen grote kathodestraalbuizen. Dit waren grote glazen buizen die beelden op het scherm projecteerden. Yttriumoxide gedoteerd met het element europium zorgde voor de rode kleur op miljoenen kleurentelevisietoestellen.
Yttriumoxide (yttria) wordt toegevoegd aan zirkoniumoxide (zirconia) om een legering te maken die de kristalstructuur van zirkoniumoxide stabiliseert. Deze structuur verandert gewoonlijk met de temperatuur. Yttria zorgt er voor dat de kubusvormige structuur van zirconiumoxide vast blijft. Hierdoor ontstaat een keramiek dat uitzonderlijk taai is en dat gebruikt kan worden bij zeer hoge temperaturen. Dit soort keramiek wordt gebruikt in een groot aantal toepassingen, van elektronica tot thermische barrièrecoatings op straalmotoren tot medische implantaten.
In de jaren ’70 werden er synthetische edelstenen gemaakt met yttriumaluminium-verbindingen die als nagemaakte diamanten en andere edelstenen werden verkocht. Uiteindelijk werden deze vervangen door kubisch zirconia. Tegenwoordig worden yttriumaluminium stenen gebruikt als kristallen die licht van industriële lasers versterken. Ook worden ze gebruikt voor microgolffilters en vinden ze toepassing in radar en communicatietechnologie.
Yttrium wordt dus voor veel toepassingen gebruikt maar het grootste gebruik is keramiek en fosfors. Kleinere hoeveelheden worden gebruikt in de metallurgie, het polijsten van glas, additieven en katalysatoren. Het wordt veel gebruikt in elektronische toepassingen maar ook vinden we het terug in zuurstofsensoren.
Yttrium wordt veel gebruikt in fosforverbindingen die worden toegepast in mobiele telefoons en grotere beeldschermen. Ook wordt het in verlichting gebruikt. Yttrium in rode fosfors in kleurentelevisiebuizen leidde tot een wijdverbreid gebruik in de jaren ’60 en ’70. Fluorescentiebuizen verbruiken aanzienlijk meer yttrium per watt dan ledlampen
Het radioactieve isotoop 90 Yt wordt gebruikt bij bestralingstherapie om leverkanker en enkele andere kankervormen te behandelen.
Huidig onderzoek
Bij de ontwikkeling van nieuwe brandstofcellen wordt gewerkt met yttrium in plaats van het veel duurdere platina. Yttrium en andere zeldzame aardmetalen worden in de vorm van nanodeeltjes gebruikt om zo de efficiëntie van elektrische auto’s te verbeteren.
Yttrium wordt gebruikt bij onderzoek naar supergeleidbaarheid. Het wordt toegepast bij apparatuur voor MRI-scans en op het gebied van zweeftreinen (levitatie). Supergeleiding bij hoge temperatuur was beperkt tot -251 °C. Toen natuurkundigen een verbinding van yttrium, barium en koperoxide ontdekten werd deze temperatuur verhoogd tot -184,4 °C. Ze hadden een materiaal gemaakt dan kon worden gekoeld met vloeibare stikstof en dit kan de kosten van toekomstige supergeleidingstoepassingen aanzienlijk verlagen.