Promethium
Inhoudsopgave
Wat is Promethium?
Promethium heeft atoomnummer 61 en symbool Pm. Het is een metaal dat zelden in de natuur voorkomt. Het is een kunstmatig en radioactief element en het behoort tot de lanthaniden. Het kan verkregen worden via splijtingsproducten van andere elementen waaronder plutonium, thorium en uranium. Het element komt in hele kleine hoeveelheden voor in uraniumertsen. Astronomen hebben promethium waargenomen in spectra van sterren in de Andromeda-nevel.
Gegevens
| Symbool | Pm |
| Volledige naam | Promethium |
| Atoomnummer | 61 |
| Atoommassa (g.mol-1 ) | 144,91 |
| Groep | Lanthaniden |
| Elektronegativiteit (Pauling) | 1,13 |
| Dichtheid (g.cm-3 bij 20 °C) | 7,22 |
| Smeltpunt (°C) | 1168 |
| Kookpunt (°C) | 2460 |
| Vanderwaalstraal (nm) | |
| Ionstraal (nm) | |
| Elektronenconfiguratie | [Xe]4f56s2 |
| Eerste ionisatiepotentiaal (kJ.mol-1) | 534,6 |
| Tweede ionisatie potentiaal (kJ.mol-1) | 1051,70 |
| Derde ionisatiepotentiaal (kJ.mol-1) | 2151,64 |
| Standaard potentiaal (V) | -2, 42 |
| Ontdekt door | Bohuslav Brauner in 1902 |
Het element is paramagnetisch en er zijn 9 isotopen bekend. Bij kamertemperatuur is promethium een vaste stof. Het heeft een kookpunt van 2460 °C. vanwege de radioactiviteit is er weinig bekend over de chemische eigenschappen van het element. Men neemt aan dat de eigenschappen overeenkomen met andere zeldzame aarden zoals cerium, scandium, europium en neodymium. Het smeltpunt is lager dan dat van samarium maar hoger dan dat van neodymium. Er zijn meer dan 30 verbindingen met promethium gemaakt waaronder verbindingen met waterstof, zuurstof en halogenen. Promethiumzouten hebben een groene of blauwe gloed.
Het element heeft geen stabiele isotopen. Promethium-151 heeft een halfwaardetijd van 1,18 dagen. De halfwaardetijd van promethium-148 is ongeveer 43 dagen. Promethium-147 is het enige isotoop met commerciële toepassingen. Alle elementen in het periodiek systeem hebben minimaal één radioactief isotoop. Echter er zijn maar twee elementen met een atoomnummer kleiner dan 83 die alleen radioactieve isotopen hebben. Dit zijn promethium en technetium.
Bohr-Rutherford diagram
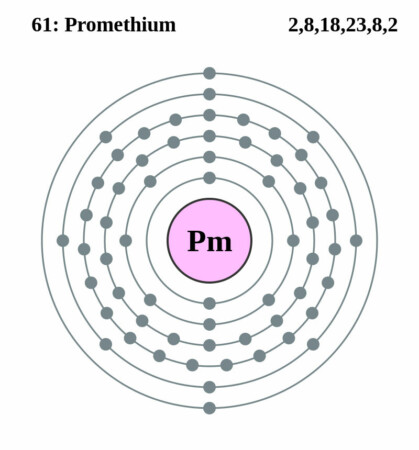
Radioisotopen
| Nuclide | Isotopische massa (u) | Halveringstijd |
|---|---|---|
| 126Pm | 125,95752 | 0,5 s |
| 127Pm | 126,95163 | 1 s |
| 128Pm | 127,94842 | 1,0 s |
| 129Pm | 128,94316 | 3 s |
| 130Pm | 129,94045 | 2,6 s |
| 131Pm | 130,93587 | 6,3 s |
| 132Pm | 131,93375 | 6,2 s |
| 133Pm | 132,92978 | 15 s |
| 134Pm | 133,92835 | 22 s |
| 135Pm | 134,92488 | 49 s |
| 136Pm | 135,92357 | 107 s |
| 137Pm | 136,92047 | 2 min |
| 138Pm | 137,91954 | 10 s |
| 139Pm | 138,91680 | 4,15 min |
| 140Pm | 139,91604 | 9,2 s |
| 141Pm | 140,91355 | 20,90 min |
| 142Pm | 141,91287 | 40,5 s |
| 143Pm | 142,91093 | 265 dagen |
| 144Pm | 143,91259 | 363 dagen |
| 145Pm | 144,91274 | 17,7 jaar |
| 146Pm | 145,91469 | 5,53 jaar |
| 147Pm | 146,91513 | 2,6234 jaar |
| 148Pm | 147,91747 | 5,368 dagen |
| 149Pm | 148,91833 | 53,08 uur |
| 150Pm | 149,92098 | 2,68 uur |
| 151Pm | 150,92120 | 28,40 uur |
| 152Pm | 151,92349 | 4,12 min |
| 153Pm | 152,92411 | 5,25 min |
| 154Pm | 153,92646 | 1,73 min |
| 155Pm | 154,92810 | 41,5 s |
| 156Pm | 155,93106 | 26,70 s |
| 157Pm | 156,93304 | 10,56 s |
| 158Pm | 157,93656 | 4,8 s |
| 159Pm | 158,93897 | 1,47 s |
| 160Pm | 159,94299 | 2 s |
| 161Pm | 160,94586 | 700 ms |
| 162Pm | 161,95029 | 500 ms |
| 163Pm | 162,95368 | 200 ms |
Toepassingen
Promethium-147 wordt gebruikt in atoombatterijen. Het element kan gebruikt worden als energiebron omdat er tijdens het verval energie vrijkomt. Promethiumbatterijen zijn een alternatief voor andere soorten batterijen die te zwaar of te groot zijn. Ze zijn een efficiënte energievoorziening in ruimtesondes en satellieten. Voor dagelijks gebruik zijn ze veel te duur. Promethiumbatterijen hebben een levensduur tot wel 5 jaar. Andere mogelijke toepassingen van promethium zijn in de fabricage van batterijen voor pacemakers, horloges en raketten.
Ontdekking
Promethium werd in 1945 ontdekt door de chemicus Jacob Marinsky. Hij gebruikte neutronen om neodymium te bombarderen en maakte op die manier promethium. Marinsky en Glendanin wisten ook promethium te extraheren uit splijtingsproducten. Het duurde tot 1963 voor het eerste promethium werd geproduceerd. Tegenwoordig gebruiken wetenschappers deeltjesversnellers om het element te isoleren.
Gezondheid & gevaar
Het element heeft geen biologische rol. Het is onbekend hoeveel promethium er op Aarde voorkomt. Uitgaande van het feit dat promethium een zeldzaam metaal is wordt aangenomen dat het geen direct gevaar vormt voor planten en dieren. Laboratoriumexperimenten hebben aangetoond dat het metaal zich opstapelt aan het oppervlak van botten. Het kost tijd om het weer uit het lichaam te verwijderen. Promethium is erg radioactief en moet voorzichtig worden behandeld. Beschermende kleding, veiligheidsbrillen en handschoenen zijn verplicht. Alle verbindingen met promethium zijn zeer giftig en metaalstof kan leiden tot een explosie of brand. Promethium komt oorspronkelijk voor op Aarde maar nu alleen nog maar als sporenelement. Dat komt door het radioactieve verval. Het element wordt alleen gebruikt in onderzoeksinstituten en nucleaire installaties.