Samarium
Inhoudsopgave
Wat is Samarium?
Samarium is een zeldzaam metaal dat tot de lanthaniden behoort. Het heeft atoomnummer 62 en symbool Sm. Samarium heeft een zilvergrijze kleur. Het ontbrandt al bij aan temperatuur van 150 °C. Samarium is voor het eerst ontdekt door de Franse chemicus Paul de Boisbaudran maar het was de Zwitserse chemicus Jean Charles Gallisard die in 1853 de eerste sporen Samarium waarnam.
Gegevens
| Symbool | Sm |
| Volledige naam | Samarium |
| Atoomnummer | 62 |
| Atoommassa (g.mol-1) | 150,35 |
| Groep | Lanthaniden |
| Elektronegativiteit (Pauling) | 1,17 |
| Dichtheid (g.cm-3 bij 20 °C) | 6,9 |
| Smeltpunt (°C) | 1074 |
| Kookpunt (°C) | 1794 |
| Vanderwaalstraal (nm) | |
| Ionstraal (nm) | |
| Isotopen | 7, waarvan 2 radioactief |
| Elektronenconfiguratie | [Xe]4f6s2 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 542,3 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1066 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 2257,77 |
| Standaard potentiaal (V) | 2,41 |
| Ontdekt door | Jean Charles Gallisard in 1853 |
Bohr-Rutherford diagram
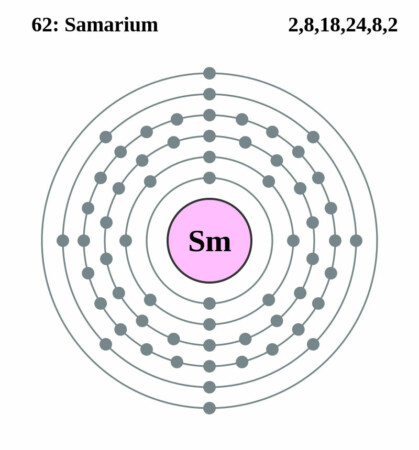
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 62 | Samarium | 144 Sm | 143,911995 | 3,07 |
| 147 Sm | 146,914893 | 14,99 | ||
| 148 Sm | 147,914818 | 11,24 | ||
| 149 Sm | 148,917180 | 13,82 | ||
| 150 Sm | 149,917271 | 7,38 | ||
| 152 Sm | 151,919728 | 26,75 | ||
| 154 Sm | 153,922205 | 22,75 |
radioisotopen
| Nuclide | Isotopische massa (u) | Halveringstijd |
|---|---|---|
| 128Sm | 127,95808 | 0,5 s |
| 129Sm | 128,95464 | 550 ms |
| 130Sm | 129,94892 | 1 s |
| 131Sm | 130,94611 | 1,2 s |
| 132Sm | 131,94069 | 4,0 s |
| 133Sm | 132,93867 | 2,90 s |
| 134Sm | 133,93397 | 10 s |
| 135Sm | 134,93252 | 10,3 s |
| 136Sm | 135,92827 | 47 s |
| 137Sm | 136,92697 | 45 s |
| 138Sm | 137,92324 | 3,1 min |
| 139Sm | 138,92229 | 2,57 min |
| 140Sm | 139,91899 | 14,82 min |
| 141Sm | 140,91847 | 10,2 min |
| 142Sm | 141,91519 | 72,49 min |
| 143Sm | 142,91462 | 8,75 min |
| 145Sm | 144,91341 | 340 dagen |
| 146Sm | 145,91304 | 1,03 * 108 jaar |
| 147Sm | 146,91489 | 1,06 × 1011 jaar |
| 148Sm | 147,91482 | 7 * 1015 jaar |
| 151Sm | 150,91993 | 90 jaar |
| 153Sm | 152,92209 | 46,284 uur |
| 155Sm | 154,92464 | 22,3 min |
| 156Sm | 155,92552 | 9,4 uur |
| 157Sm | 156,92836 | 8,03 min |
| 158Sm | 157,92999 | 5,30 min |
| 159Sm | 158,93321 | 11,37 s |
| 160Sm | 159,93514 | 9,6 s |
| 161Sm | 160,93883 | 4,8 s |
| 162Sm | 161,94122 | 2,4 s |
| 163Sm | 162,94536 | 1 s |
| 164Sm | 163,94828 | 500 ms |
| 165Sm | 164,95298 | 200 ms |
Eigenschappen
Samarium is een zacht metaal met paramagnetische eigenschappen. In lucht is het stabiel en bij kamertemperatuur is het een vaste stof. Bij hogere luchtvochtigheden ontstaat er een oxidelaagje aan het oppervlak. Als het oxideert dan ontstaat er een geel-grijs poeder bestaande uit oxides en hydroxides. Het metaal kan het beste onder argon of een ander inert gas worden bewaard. Er zijn 21 isotopen bekend. Samarium kan verschillende verbindingen vormen waaronder borides, halides, chalcogenides en oxides. Het element heeft nucleaire isomeren en radioisotopen en stabiele isotopen als Sm-154, Sm-152, Sm-150 en Sm-144. Enkele isotopen hebben een halfwaardetijd van 340 dagen maar bijvoorbeeld Sm-153 heeft een halfwaardetijd van slechts 1,92 dagen.
Bronnen, ertsen & toepassingen
Het metaal komt voor in verschillende mineralen zoals monaziet, samarskiet en gadoliniet. Het wordt ook gevonden in ceriet, bastaniet en andere mineralen. Ertsen die samarium bevatten worden gevonden in landen als Australië, Sri Lanka, India, Brazilië, de Verenigde Staten en China.
Er worden verschillende winnings- en zuiveringstechnieken toegepast. Samarium wordt o.a. toegepast in kernreactoren en optische lasers. Het metaal wordt ook als reductor gebruikt bij verschillende soorten reacties zoals de barbierreactie, de Holton Taxolsynthese, Danishefsky en anderen.
Het element wordt ook gebruikt in de elektronica- en de keramische industrie. Het wordt toegepast in katalysatoren en speciale glassoorten. Samarium heeft toepassingen in de radiografie, interferometrie, hoge resolutiemicroscopie, holografie en meer. Sommige isotopen worden gebruikt om de ouderdom van meteorieten en gesteente te bepalen. Samarium wordt ook toegepast in hoofdtelefoons, legeringen met kobalt, lasers, organische reagentia en koolstoflampen. In de jaren ’70 werden samarium-kobaltmagneten gebruikt om de grootte van luidsprekers etc. te verkleinen.
Magneten met samarium zijn duur maar krachtig. Samariummagneten kunnen nog bij hoge temperaturen worden gebruikt. Ze worden tegenwoordig veel in elektrische auto’s toegepast. Samariummagneten worden ook in de industrie toegepast daar waar een laag energieverbruik vereist is.
Samariumkobaltmagneten hebben een goede spectrale absorptie en worden daarom ook toegepast in applicaties die microgolffrequenties gebruiken.
Samarium wordt ook in de geneeskunde gebruikt. Enkele behandelingen tegen kanker maken gebruik van het radio-isotoop Sm-153. Samarium wordt ook gebruikt om, in combinatie met neodymium, cerium en lanthaan, vuursteentjes te maken. Als samarium wordt gehydrateerd met ethanol dan kan het als katalysator worden gebruikt.
Gezondheid & Gevaar
Samarium versnelt het metabolisme. In het menselijk lichaam wordt samarium aangetroffen in de bloedsomloop, nieren en lever. Blootstelling aan grote hoeveelheden samariumzouten leidt tot oog- en huidirritatie. Het metaal is ook in sommige planten en dieren aangetroffen.