Bismut
Inhoudsopgave
Bismut is een bros, kristallijn wit metaal net een licht roze tint. Het heeft een verscheidenheid aan toepassingen waaronder cosmetica, legeringen, brandblussers en munitie. Het is waarschijnlijk het best bekend als het belangrijkste ingrediënt in remedies tegen buikpijn.
Bismut is element 83 in het periodiek systeem der elementen. Het is een post-transitiemetaal maar het wordt soms ook wel bij de transitiemetalen gerekend. Transitiemetalen zijn de grootste groep elementen, ook koper, ijzer, lood, zink en goud behoren ertoe. Transitiemetalen zijn hard, ze hebben hoge smeltpunten en kookpunten. Post-transitiemetalen hebben enkele overeenkomsten met de transitiemetalen maar ze zijn zachter en het zijn slechtere geleiders. De elektrische en thermische geleidbaarheid van bismut is ongebruikelijk laag voor een metaal. Bismut heeft ook een laag smeltpunt waardoor het in legeringen gebruikt kan worden die gebruikt worden in brandblussers, brandmelders en gietmallen.
Tot redelijk recent werd bismut beschouwt als het zwaarste metaal met een stabiele kern. Echter in 2003 ontdekten wetenschappers dat bismut vervalt naar thallium maar dat het een extreem lange halfwaardetijd heeft van ongeveer 19 triljoen jaar (1,9 * 1019 jaar). Anders gezegd, als 100 gram 209Bi (de natuurlijke isotoop) meer dan 14 miljard jaar geleden aan het begin van het heelal aanwezig was geweest dan zou daar vandaag nog ongeveer 99,9999999 gram van over zijn. Tegenwoordig is lood het zwaarste stabiele element.
Chemische gegevens
| Symbool | Bi |
| Volledige naam | Bismut |
| Atoomnummer | 83 |
| Atoommassa (g.mol-1 ) | 208,98040 |
| Groep | post-transitiemetaal |
| Elektronegativiteit (Pauling) | 2,02 |
| Dichtheid (g.cm-3 bij 20 °C) | 9,78 |
| Smeltpunt (°C) | 271,5 |
| Kookpunt (°C) | 1564 |
| Vanderwaalsstraal (nm) | 207 |
| Ionstraal (nm) | |
| Isotopen | 1 natuurlijk |
| Elektronenschil | [Xe]4f145d106s26p3 |
| Elektronen per schil | 2, 8, 18, 32, 18, 5 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 703 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1610 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 2466 |
| Standaard potentiaal (V) | — |
| Ontdekt door: | 1753 door Claude Joffrey de Jonge |
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 83 | Bismut | 209 Bi | 208,980383 | 100 |
radioisotopen
| Nuclide | Isotopische massa (u) | Halveringstijd |
|---|---|---|
| 184Bi | 184,00112 | 6,6 ms |
| 185Bi | 184,99763 | 2 ms |
| 186Bi | 185,99660 | 14,8 ms |
| 187Bi | 186,99315 | 32 ms |
| 188Bi | 187,99227 | 44 ms |
| 189Bi | 188,98920 | 674 ms |
| 190Bi | 189,9883 | 6,3 s |
| 191Bi | 190,98578 | 12,3 s |
| 192Bi | 191,98546 | 34,6 s |
| 193Bi | 192,98296 | 67 s |
| 194Bi | 193,98283 | 95 s |
| 195Bi | 194,98065 | 183 s |
| 196Bi | 195,98066 | 5,1 min |
| 197Bi | 196,97886 | 9,33 min |
| 198Bi | 197,97921 | 10,3 min |
| 199Bi | 198,97767 | 27 min |
| 200Bi | 199,97813 | 36,4 min |
| 201Bi | 200,97700 | 108 min |
| 202Bi | 201,97774 | 1,72 uur |
| 203Bi | 202,97687 | 11,76 uur |
| 204Bi | 203,97781 | 11,22 uur |
| 205Bi | 204,97738 | 15,31 dagen |
| 206Bi | 205,97849 | 6,243 dagen |
| 207Bi | 206,97847 | 32,9 jaar |
| 208Bi | 207,97974 | 3,68 × 105 jaar |
| 209Bi | 208,98039 | 1,9 × 1019 jaar |
| 210Bi | 209,98412 | 5,012 dagen |
| 211Bi | 210,98726 | 2,14 min |
| 212Bi | 211,99128 | 60,55 min |
| 213Bi | 212,99438 | 45,59 min |
| 214Bi | 213,99871 | 19,9 min |
| 215Bi | 215,00177 | 7,6 min |
| 216Bi | 216,00630 | 2,17 min |
| 217Bi | 217,00947 | 98,5 s |
| 218Bi | 218,01432 | 33 s |
Bohr – Rutherford diagram
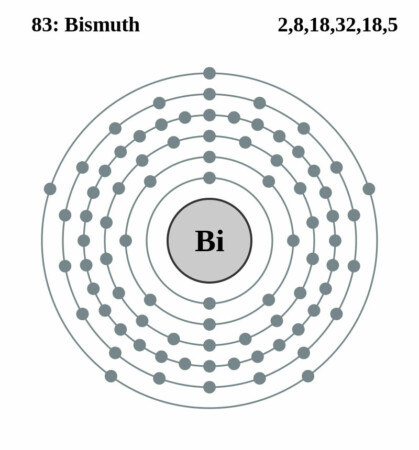
Ontdekking
Bismut is al sinds 1400 bekend maar omdat het een gelijkaardig metaal met een laag smeltpunt is als lood werd het daar vaak mee verward. De Franse chemicus Claude Geoffrey de Jonge was in 1753 de eerste die bewees dat bismut verschilt van lood.
Het woord “bismut” is een gelatineerde versie van een oud-Duits woord “weismuth” of “witte substantie”, mogelijk genoemd naar het witte oxide van het element.
Bronnen
Natuurlijk voorkomend bismut wordt in kleine hoeveelheden in de aardkorst aangetroffen, zowel als zuiver metaal als in combinatie met andere elementen in verschillende verbindingen. De grootste bron van bismut wordt gevonden in het mineraal bismutiniet of bismutsulfide (Bi2S3). Bismut wordt meestal verkregen als bijproduct bij het zuiveren van lood-, koper-, tin-, zilver- en gouderts uit Bolivia, Peru, Japan, Mexico en Canada.
Eigenschappen
Vergeleken met andere metalen is bismut het meest diamagnetisch. Dit wil zeggen dat het bestand is tegen magnetisering en wordt afgestoten door een magnetisch veld. Het heeft een lage elektrische geleidbaarheid en de grootste elektrische weerstand wanneer het in een magneetveld wordt geplaatst. Dit wordt het Hall-effect genoemd.
Bismut heeft een erg lage thermische geleidbaarheid, uitgezonderd kwik lager dan welk ander element dan ook. Het heeft ook een relatief laag smeltpunt, vooral wanneer het wordt gelegeerd met tin en lood. Bismut brandt met een blauwe vlam en bij verhitting komen er wolken van geel oxide vrij.
Als vloeibaar bismut bevriest dan zet het uit in plaats van samen te trekken. Dit komt omdat het een kristallijne structuur heeft die lijkt op water. Vier andere elementen zetten ook uit als ze bevriezen: silicium, gallium, antimoon en germanium. Bismutkristallen zijn gemakkelijk thuis te maken. Er staan verschillende handleidingen online.
Bismut in je medicijnkastje
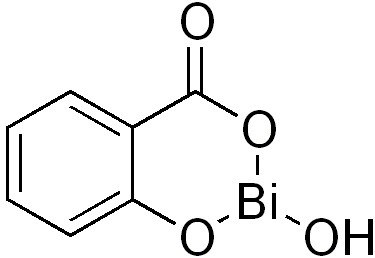
Bismutsubsalicylaat (C7H5BiO4) is een bekend middel tegen buikpijn en diarree. Het werkt door de stroom van vloeistoffen en elektrolyten in de darm te verminderen. Het vermindert ontstekingen in de darm en kan de organismen doden die diarree kunnen veroorzaken.
Veel cosmetica, waaronder lippenstift, oogschaduw en nagellak bevat bismutoxychloride (BiOCl). Dit is een parelmoerpoeder dat de producten laat glanzen,
Industrieel en militair gebruik
Bismutverbindingen worden als katalysator gebruikt bij de productie van synthetische vezels en rubber.
Als bismut wordt gecombineerd met andere metalen zoals lood, tin en cadmium vormt het legeringen met een laag smeltpunt die gebruikt kunnen worden in branddetectoren en blussers.
Omdat het vloeibare metaal 3,32% uitzet als hij vloeibaar wordt worden legeringen van bismut worden ook gebruikt bij het maken van gietstukken van voorwerpen die onderhevig zijn aan beschadiging bij hoge temperaturen
Bismanol, een legering van bismut en mangaan, is een permanente magneet met een hoge coërcitiekracht (een maat voor demagnetisatie) die in de jaren vijftig is ontwikkeld. Het werd vooral in kleine motoren gebruikt.
Bismut wordt gebruikt als vervanging van lood in kogels.
Bismut kan ook gebruikt worden in kernreactoren en om transuranium-elementen te maken met behulp van een proces dat koude kernfusie wordt genoemd.