Wat zijn isotopen?
Een familie van mensen bestaat uit aan elkaar gerelateerde maar niet identieke individuen. Ook elementen hebben families, we noemen ze isotopen. Isotopen zijn leden van een familie van een element die allemaal hetzelfde aantal protonen hebben maar een verschillend aantal neutronen.
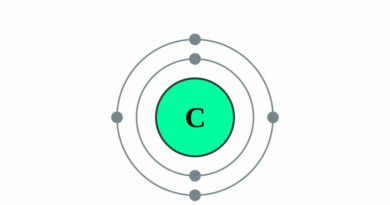
Het aantal protonen in de kern bepaalt het atoomnummer van het element in het periodiek systeem. Als voorbeeld: koolstof heeft 6 protonen en heeft dus atoomnummer 6. Koolstof komt van nature voor in drie isotopen: koolstof 12 met 6 neutronen (en zes protonen = 12), koolstof 13 met 7 neutronen en 6 protonen en koolstof 14 met 8 neutronen en 6 protonen. Ieder element heeft zijn eigen aantal isotopen.
De toevoeging van slechts één neutron kan de eigenschappen van een isotoop al drastisch veranderen. Zo is koolstof 12 stabiel. Dit betekent dat er geen radioactief verval optreedt. Koolstof 14 is niet stabiel, het ondergaat radioactief verval en het heeft een halfwaardetijd van 5730 jaar (dit betekent dat na 5730 jaar de helft van het materiaal is verdwenen). Dit verval betekent dat de hoeveelheid koolstof 14 werkt als een klok die de leeftijd van een object toont. We noemen dit koolstofdatering.
Isotopen hebben unieke eigenschappen die ze bruikbaar maken in de diagnostiek en behandeling van ziektes. Ze zijn belangrijk in nucleaire medicijnen, olie- en gaswinning, research en de nationale veiligheid.
Feitjes
- Alle elementen hebben isotopen
- Er zijn twee hoofgroepen te onderscheiden: stabiele en niet stabiele (radioactieve) isotopen
- Er zijn 254 bekende stabiele isotopen
- Alle kunstmatige (in een lab gemaakte) isotopen zijn niet stabiel en daarom radioactief: ze worden door chemici radio-isotopen genoemd.
- Sommige elementen komen alleen in een niet stabiele vorm voor (bijvoorbeeld uranium)
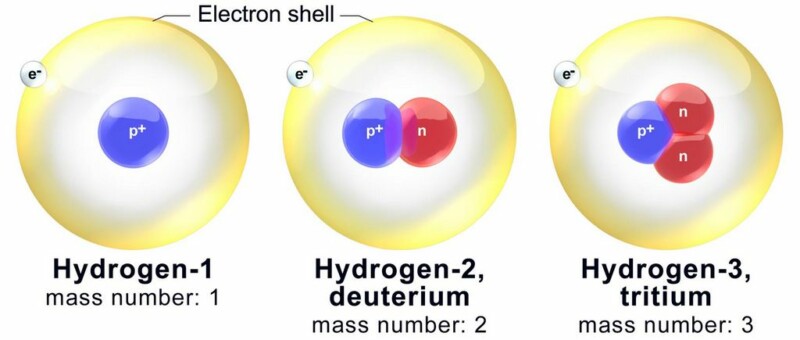
- Waterstof is het enige element waarvan de isotopen unieke namen hebben: deuterium voor waterstof met 1 neutron en tritium voor waterstof met 2 neutronen.
Petten
Wereldwijd zijn er slechts 6 reactoren waar isotopen worden geproduceerd. Deze isotopen worden voornamelijk voor nucleaire medicijnen gebruikt. De reactor in het Noord-Hollandse Petten is verantwoordelijk voor ongeveer 35% van de wereldwijde productie van isotopen. Binnen Europa is dit zelfs 65%.