Dysprosium
Inhoudsopgave
Wat is Dysprosium?
Dysprosium heeft atoomnummer 66 en symbool Dy. Het behoort tot de zeldzame aardmetalen. Dysprosium komt niet vrij voor in de natuur. Er zijn 7 isotopen bekend van dysprosium. Dysprosium werd in 1884 door de Franse chemicus Boisbaudran ontdekt als een verontreiniging in erbiumoxide. In 1906 werd het geïsoleerd door de Franse chemicus Georges Urbain maar het duurde tot de jaren ’50 toen de Canadese chemicus Frank Spedding en zijn team er in slaagde om met behulp van ionenuitwisseling en metallografische reductietechnieken zuiver dysprosium te maken.
Gegevens
| Symbool | Dy |
| Volledige naam | Dysprosium |
| Atoomnummer | 66 |
| Atoommassa (g.mol-1 ) | 162,50 |
| Groep | Lanthaniden |
| Elektronegativiteit (Pauling) | 1,2 |
| Dichtheid (g.cm-3 bij 20 °C) | 8,6 |
| Smeltpunt (°C) | 1412 |
| Kookpunt (°C) | 2562 |
| Vanderwaalstraal (nm) | |
| Ionstraal (nm) | |
| Isotopen | 12 |
| Elektronenconfiguratie | [Xe]4f106s2 |
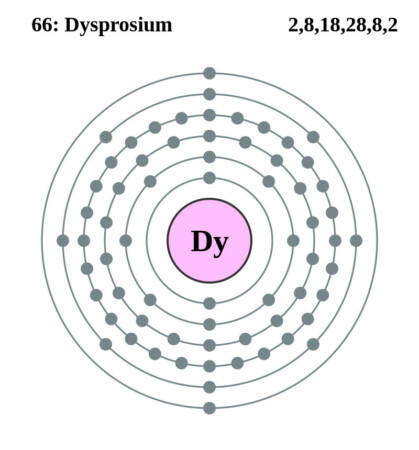
| Elektronen per schil | 2, 8, 18, 28, 8, 2 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 571,2 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1124 |
| Derde Ionisatiepotentiaal (kJ.mol-1 ) | 2199,88 |
| Standaard potentiaal (V) | -2,35 |
| Ontdekt door | Paul Emile Lecoq de Boisbaudran in 1886 |
Herkomst woord
Dysprosium stamt af van het Griekse woord “Dysprositos” en dat betekent “moeilijk te bereiken”.
Bohr-Rutherford diagram
Dysprosium komt voor in fergusoniet, xenotiem, blomstandien, euxeniet, gadoliniet, polycrase en andere mineralen. Het meeste dysprosium wordt gewonnen in het zuiden van China.
Dysprosium wordt voornamelijk gewonnen uit monaziet zand. Dit is een verbinding bestaande uit veel verschillende fosfaten. Het metaal wordt verkregen als bijproduct bij de extractie van yttrium en het wordt geïsoleerd met behulp van magnetische processen.
De wereldwijde jaarproductie bedraagt ongeveer 100 ton metaal. Dysprosium speelt een belangrijke rol bij nieuwe opkomende technologieën voor schone energie. Voor de toekomst worden er grote tekorten voorspeld.
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 66 | Dysprosium | 156 Dy | 155,924278 | 0,06 |
| 158 Dy | 157,924405 | 0,10 | ||
| 160 Dy | 159,925194 | 2,34 | ||
| 161 Dy | 160,926930 | 18,91 | ||
| 162 Dy | 161,926795 | 25,51 | ||
| 163 Dy | 162,928728 | 24,90 | ||
| 164 Dy | 163,929171 | 28,18 |
Radioisotopen
| Nuclide | Isotopische massa (u) | Halfwaardetijd |
|---|---|---|
| 138Dy | 137,96249 | 200 ms |
| 139Dy | 138,95954 | 600 ms |
| 140Dy | 139,95401 | 700 ms |
| 141Dy | 140,95135 | 0,9 s |
| 142Dy | 141,94637 | 2,3 s |
| 143Dy | 142,94383 | 5,6 s |
| 144Dy | 143,93925 | 9,1 s |
| 145Dy | 144,93743 | 9,5 s |
| 146Dy | 145,93284 | 33,2 s |
| 147Dy | 146,93109 | 40 s |
| 148Dy | 147,92715 | 3,3 min |
| 149Dy | 148,92730 | 4,20 min |
| 150Dy | 149,92558 | 7,17 min |
| 151Dy | 150,92618 | 17,9 min |
| 152Dy | 151,92471 | 2,38 uur |
| 153Dy | 152,92576 | 6,4 uur |
| 154Dy | 153,92442 | 3,0 * 106 jaar |
| 155Dy | 154,92575 | 9,9 uur |
| 157Dy | 156,92546 | 8,14 uur |
| 159Dy | 158,92573 | 144,4 dagen |
| 165Dy | 164,93170 | 2,334 uur |
| 166Dy | 165,93280 | 81,6 uur |
| 167Dy | 166,93566 | 6,20 min |
| 168Dy | 167,93713 | 8,7 min |
| 169Dy | 168,94031 | 39 s |
| 170Dy | 169,94239 | 30 s |
| 171Dy | 170,94620 | 6 s |
| 172Dy | 171,94876 | 3 s |
| 173Dy | 172,95300 | 2 s |
Eigenschappen
Dysprosium maakt deel uit van de lanthaniden en het is een helder zilverkleurig element. Bij kamertemperatuur is het redelijk stabiel. Het lost gemakkelijk op in minerale zuren. Hierbij komt waterstof vrij. Kleine hoeveelheid verontreinigingen kunnen de eigenschappen van het element snel veranderen maar in het algemeen is Dysprosium zacht genoeg om met een mes te snijden.
Toepassingen
Dysprosium kan gebruikt worden in controlestaven van kernreactoren en zijn magnetische eigenschappen maken het ook voor datadragers. Dysprosium heeft een hoog smeltpunt en het absorbeert gemakkelijk neutronen. In een legering met staal wordt het daarom ook toegepast in kernreactoren. Dysprosia of dysprosiumoxide wordt gebruikt om buizen in kernreactoren te koelen. Hiervoor wordt dysprosium gemengd met nikkel en toegevoegd aan een speciale cementsoort. Andere verbindingen van dysprosium zijn dysprosiumsulfaat, dysprosiumjodide en dysprosiumfluoride.
Een klein gedeelte van de samenstelling van neodymium-ijzer-boor magneten kan vervangen worden door dysprosium. Dit leidt tot een grotere energiecapaciteit in hybride elektrische auto’s. Per auto zou het gaan om ongeveer 100 gram dysprosium. Dat klinkt als niet veel maar uitgaande van de enorme markt voor hybride auto’s betekent dit dat er wereldwijd snel een tekort van dysprosium zou kunnen optreden.
Dysprosium wordt ook toegepast in dosimeters, katalysatoren en verlichting die een hoge intensiteit moet hebben. Voor dit laatste worden dysprosiumbromide en dysprosiumjodide gebruikt. Deze verbindingen geven dysprosiumionen af die zorgen voor helder licht.
Dosimeters worden gebruikt om de hoeveelheid ioniserende straling te meten. Dit gebeurt door met mengen van het metaal met calciumsulfaat of calciumfluoride. Als deze aan straling worden blootgesteld dan wordt dysprosium lichtgevend en dat kan worden gebruikt als een indicator om te bepalen waar de dosimeter aan is blootgesteld.