Rutherfordium
Inhoudsopgave
Rutherfordium is vernoemd naar de chemicus Ernest Rutherford.
Ontdekking
Er is enige controverse geweest over de ontdekking van rutherfordium. Het werd voor het eerst gerapporteerd door een team van wetenschappers in Dubna, Rusland in 1964. Ze identificeerden een isotoop, 260Rf, met een gerapporteerde halfwaardetijd van 0,3 seconden. Ze veranderden later het rapport met hun bevindingen en stelden dat 260Rf een halfwaardetijd van 0,15 seconden had. In 1969 probeerde een team van wetenschappers van de universiteit van Californië in Berkeley de resultaten van het Dubna-team te reproduceren. Ze gebruikten een andere methode. De Amerikanen produceerden 4 isotopen van rutherfordium maar de rapporten over of ze ook daadwerkelijk 260Rf hadden gemaakt, variëren. Dat geldt ook voor de officiële erkenning van welk team nu het element als eerste heeft ontdekt.
Eigenschappen
Rutherfordium is een synthetisch element en er is weinig bekend over de eigenschappen. Aangenomen wordt dat het een massief metaal is. Het is het eerste trans-actinide element en er wordt aangenomen dat het chemische eigenschappen heeft die vergelijkbaar zijn met die van hafnium.
Rutherfordium heeft 13 erkende isotopen met bekende halfwaardetijden. Het meest stabiele isotoop is 263Rf dat een halfwaardetijd heeft van 10 minuten. Het vervalt door spontane splijting.
Chemische gegevens
| Symbool | Rf |
| Volledige naam | Rutherfordium |
| Atoomnummer | 104 |
| Atoommassa (g.mol-1 ) | 267 |
| Groep | transitie metaal |
| Elektronegativiteit (Pauling) | |
| Dichtheid (g.cm-3 bij 20 °C) | 23,2 |
| Smeltpunt (°C) | 2100 |
| Kookpunt (°C) | 5500 |
| Vanderwaalsstraal (nm) | |
| Ionstraal (nm) | |
| Isotopen | 13 |
| Elektronenschil | [Rn]5f146d27s2 |
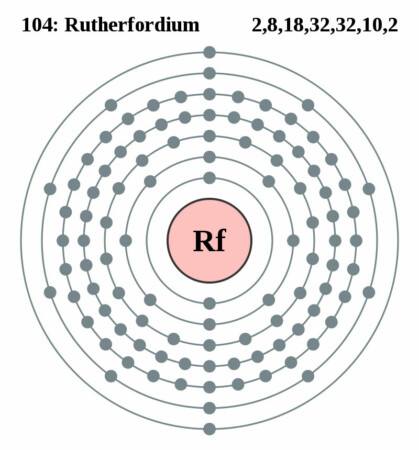
| Elektronen per schil | 2, 8, 18, 32, 32, 10, 2 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | — |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | — |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | — |
| Standaard potentiaal (V) | — |
| Ontdekt door: | 1964 Joint Institute for Nuclear Research, Dubna en 1969 Lawrence Berkeley National Laboratory, Californië |
Bohr – Rutherford diagram
Radioisotopen
| Nuclide | Isotopische massa (u) | Halfwaardetijd |
|---|---|---|
| 253Rf | 253,10069 | 13 ms |
| 255Rf | 255,10134 | 1,64 s |
| 256Rf | 256,10116 | 6,45 ms |
| 257Rf | 257,10299 | 4,7 s |
| 258Rf | 258,10349 | 12 ms |
| 259Rf | 259,10564 | 2,8 s |
| 260Rf | 260,10644 | 21 ms |
| 261Rf | 261,10877 | 5,5 s |
| 262Rf | 262,10993 | 2,3 s |
| 263Rf | 263,11255 | 11 min |
| 266Rf | 266,11796 | 10 uur |
| 267Rf | 267,12153 | 5 uur |
| 268Rf | 268,12364 | 1 uur |
Bronnen
Rutherfordium wordt kunstmatig geproduceerd en er zijn slechts kleine hoeveelheden van gemaakt. De Dubna-wetenschappers produceerden het door plutonium te bombarderen met tot 113 – 115 MeV versnelde neonionen. Het Berkeley-team produceerde vier isotopen door 249Cf te bombarderen met 12C-kernen van 71 MeV en 13C-kernen van 69 MeV.
Toepassingen
Er zijn slechts kleine hoeveelheden rutherfordium geproduceerd en de isotopen ervan hebben allemaal een zeer korte halfwaardetijd. Om deze reden wordt het alleen gebruikt voor wetenschappelijk onderzoek.