Fluor
Inhoudsopgave
Wat is Fluor?
Fluor heeft atoomnummer 9 en symbool F. Normaal is fluor een gas met een lichtgele kleur dat bestaat uit diatomaire moleculen, F2. Fluor komt op Aarde meer voor dan in sterren. Hier op Aarde is fluor het 13de meest voorkomende element in de korst van de Aarde. Fluor is het lichtste element van de halogenen. Halogenen zijn niet-metaal elementen. De andere halogenen zijn chloor (Cl), jood (I), broom (Br) en astatine (At). Bij kamertemperatuur komen ze allemaal in alle drie de aggregatietoestanden voor. De halogenen zijn in dit opzicht uniek.
Chemische gegevens
| Symbool | F |
| Volledige naam | Fluor |
| Atoomnummer | 9 |
| Atoommassa (g.mol-1 ) | 18,998403 |
| Elektronegativiteit (Pauling) | 4 |
| Dichtheid (g.cm-3 bij 20 °C) | 1,8 * 10-3 |
| Smeltpunt (°C) | -219,6 |
| Kookpunt (°C) | -188 |
| Vanderwaalsstraal (nm) | 0,135 |
| Ionstraal (nm) | 0,136 (-1); 0,007 (+7) |
| Isotopen | 1 |
| Elektronenconfiguratie | [He]2s2 2p5 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 1680 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 3374 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 6050 |
| Standaard potentiaal (V) | -2,87 |
| Ontdekt | Henri Moissan in 1886 |
Fluor heeft één natuurlijk isotoop; Fluor-19. De andere isotopen zijn niet stabiel. Fluor is een hele sterke oxidator en dat komt omdat het, op chloor na, het meeste aantal elektronen aantrekt. De verbindingen die fluor met alle andere elementen, op neon en helium na, vormt worden fluorides genoemd. Alhoewel zwakker dan zoutzuur is waterstoffluoride erg corrosief.
De verbindingen met fluor zijn o.a. metaalfluoriden, organische verbindingen met fluor en nog veel meer. De eerste zijn meestal ionische zouten die meestal oplosbaar zijn in water. Organische fluorverbindingen zijn meestal zeer stabiel, zowel chemisch als thermisch. Ze zijn waterafstotend en hebben een relatief laag smelt- en kookpunt. Sommige van die verbindingen worden op grote schaal gebruikt zoals fluorkoolwaterstofgassen die worden gebruikt om te koelen en vriezen of bijvoorbeeld teflon.
Vanwege het zeer reactieve karakter komt fluor niet van nature voor. De naam is afgeleid van het Latijnse werkwoord “fluo” en dat betekent “vloeien”. Dit komt omdat fluoriet het smeltpunt van bepaalde ertsen verlaagd als het wordt toegevoegd. Voor 1886 was fluor alleen bekend als mineraal. In dat jaar werd het als element herkent door de Frans chemicus Henri Moissan. Hij is ook bekend om zijn ontdekking van de elektrolyse methode in de industriële productie.
Bohr-Rutherford diagram
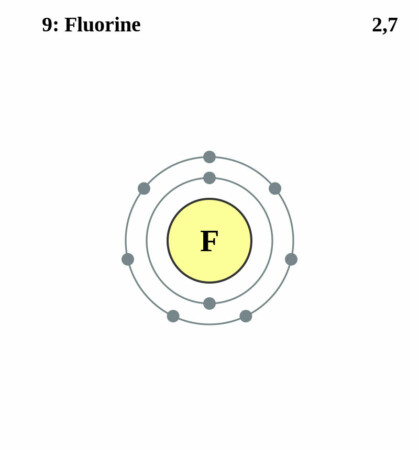
By Pumbaa (original work by Greg Robson) – CC BY-SA 2.0 uk,
Isotopen
| Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|
| Fluor | 19 F | 18,998403 | 100 |
Radioisotopen
| Symbool | Atoommassa (u) | Halfwaardetijd |
|---|---|---|
| 14F | 14,03432 | 500 * 10-24 s |
| 15F | 15,017785 | 1,1 * 10-21 s |
| 16F | 16,011466 | 11 * 10-21 s |
| 17F | 17,00209524 | 64,370 s |
| 18F | 18,0009373 | 109,739 min |
| 20F | 19,99998125 | 11,163 s |
| 21F | 20,9999489 | 4,158 s |
| 22F | 22,002999 | 4,23 s |
| 23F | 23,00353 | 2,23 s |
| 24F | 24,00810 | 384 ms |
| 25F | 26,01217 | 80 ms |
| 26F | 26,02002 | 8,2 ms |
| 27F | 27,02732 | 4,9 ms |
| 28F | 28,03622 | 46 * 10-21 s |
| 29F | 29,04310 | 2,5 ms |
| 31F | 31,06027 | >260 ns |
Spectra
Absorptiespectrum
Emissiespectrum
Toepassingen
Commercieel wordt fluor toegepast in tandpasta’s. Het helpt bij het voorkomen van tandbederf. Sommige verbindingen van het element maar ook het element zelf zijn giftig. Dat neemt niet weg dat fluor en fluorverbindingen veel in de farmaceutische industrie worden toegepast.
In sommige landen worden fluor toegevoegd aan het drinkwater met als doel tandbederf te voorkomen. Er worden ook andere fluorverbindingen, zoals natrium monofluorofosfaat, tin(II)fluoride en natriumfluoride, toegevoegd aan tandpasta.
Waterstoffluoride wordt gebruikt om glas te etsen waaronder glas dat voor gloeilampen wordt gebruikt. Uraniumhexafluoride wordt gebruikt voor het scheiden van uraniumisotopen. Kristallen van calciumfluoride en fluoriet worden gebruikt om er lenzen van te maken die infrarood licht kunnen bundelen. Sommige verbindingen, zoals bijvoorbeeld dichlorodifluoromethaan werden algemeen gebruikt in koelsystemen en airconditioners maar ook als drijfgas in spuitbussen. Omdat dergelijke verbindingen de ozonlaag aantasten worden ze tegenwoordig niet meer gebruikt. Gecombineerd met koolstof vormt fluor verbindingen die bekend zijn als fluorkoolstoffen.
Fluoratomen hebben negen protonen en negen elektronen. De buitenste elektronen hebben een lading van +7. Het element heeft de neiging om een elektron op te nemen waarmee fluor het meest elektronegatieve element is dat we kennen. Het kost enorm veel energie om een elektron uit een fluoratoom te verwijderen.
De mineralen fluoriet, fluorapatiet en cryoliet zijn de meest voorkomende mineralen die fluor bevatten die in de industrie worden gebruikt.