Chloor
Inhoudsopgave
Wat is Chloor?
Chloor, atoomnummer 17 en symbool Cl, behoort tot de halogenen. Het is een giftig groengeel gas. Het komt in de natuur veel voor in de vorm van natriumchloride dat we vooral terugvinden in zeewater. Een andere naam voor natriumchloride is tafelzout. Het chloride-ion zelf maakt deel uit van het zout in de Aarde en in de oceanen. In feite bestaat bijna 2% van de zeewatermassa uit chloride-ionen. In de superzoute Dode Zee is dit met 34% nog veel meer.
Chemische gegevens
| Symbool | Cl |
| Volledige naam | Chloor |
| Atoomnummer | 17 |
| Atoommassa (g.mol-1 ) | 35,453 |
| Groep | Halogenen |
| Elektronegativiteit (Pauling) | 3,0 |
| Dichtheid (g.cm-3 bij 20 °C) | 3,21 * 10-3 |
| Smeltpunt (°C) | -101 |
| Kookpunt (°C) | -34,6 |
| Vanderwaalstraal (nm) | 0,127 |
| Ionstraal (nm) | 0,184 (-2); 0,029 (+6) |
| Isotopen | 2 |
| Elektronenconfiguratie | [Ne]3s2 3p5 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 1255,7 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 2297,72 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 3821,81 |
| Standaard potentiaal (V) | -1,36 |
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 17 | Chloor | 35 Cl | 34,968853 | 75,78 |
| 37 Cl | 36,965903 | 24,22 |
Radioisotopen
| Symbool | Atoommassa (u) | Halfwaardetijd |
| 28 Cl | 28,02851 | onbekend |
| 29 Cl | 29,01411 | < 20 ns |
| 30 Cl | 30,00477 | < 30 ns |
| 31 Cl | 30,99241 | 150 ms |
| 32 Cl | 31,985690 | 298 ms |
| 33 Cl | 32,9774519 | 2,511 s |
| 34 Cl | 33,97376282 | 1,5264 s |
| 36 Cl | 35,96830698 | 3,01 * 105 jaar |
| 38 Cl | 37,96801043 | 37,24 min |
| 39 Cl | 38,9680082 | 55,6 min |
| 40 Cl | 39,97042 | 1,35 min |
| 41 Cl | 40,97068 | 38,4 s |
| 42 Cl | 41,97325 | 6,8 s |
| 43 Cl | 42,97405 | 3,07 s |
| 44 Cl | 43,97828 | 0,56 s |
| 45 Cl | 44,98029 | 400 ms |
| 46 Cl | 45,98421 | 232 ms |
| 47 Cl | 46,98871 | 101 ms |
| 48 Cl | 47,99495 | 100 ms |
| 49 Cl | 49,00032 | 50 ms |
| 50 Cl | 50,00784 | 20 ms |
| 51 Cl | 51,01449 | 2 ms |
Bohr-Rutherford diagram
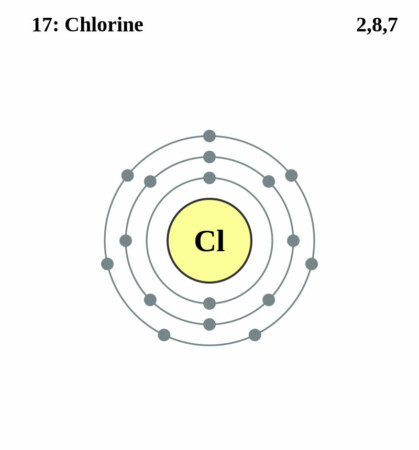
By Pumbaa (original work by Greg Robson) – Application: (generated by script), CC BY-SA 2.0 uk,
Spectra
Absorptiespectrum
Emissiespectrum
Chloor is in 1774 ontdekt door Karl Scheele en het werd in 1810 als element door Humprey David bevestigd.
Omdat chloride in het algemeen goed oplosbaar is in water, worden grote hoeveelheden stoffen die chloride bevatten meestal alleen gevonden in droge klimaten of diep onder de grond, zoals in de aardkorst. Chloor is daar in zeer hoge concentraties aanwezig. Het komt vooral voor in mineralen als haliet, sylviet en carnalliet.
Chloor heeft verschillende isotopen. De belangrijkste zijn 35Cl (75,77%) en 37Cl (24,23%). Ze zorgen voor het atoomgewicht van het element dat 35,4527 g*mol-1 bedraagt.
Chloor heeft een zeer belangrijke wetenschappelijke functie, het kan namelijk gebruikt worden voor geologische datering. Chloor heeft een halfwaardetijd van 308.000 jaar. Dit betekent dat er twee keer zoveel jaren voorbij moeten gaan voordat de sporen er van in het milieu zijn verdwenen. Het kan ook gebruikt worden om wateren minder dan 50 jaar oud te dateren. Het is gebruikt voor het dateren van ijs en sedimenten.
Het amylase-ion bevat een chloride-ion, terwijl calciumchloride, een verbinding van chloor, wordt gebruikt om de vochtigheid in ruimtes te verlagen. Calciumchloride heeft nog andere toepassingen zoals het gebruik in de wegenbouw.
Chloor wordt veel gebruikt in de industrie en in huishoudelijke producten. In de vorm van gas kan chloor zeer gevaarlijk zijn. Om chloorgas te kunnen vervoeren wordt het onder druk gebracht zodat het vloeibaar wordt en als de vloeistof weer vrijkomt dan verandert het in een gas dat zich zeer snel kan verspreiden. Het heeft een doordringende, onaangename geur, zoals die van bleekwater. Deze geur kan een voordeel zijn omdat het mensen kan waarschuwen voor de aanwezigheid van het gas. Een ander waarschuwingsteken is de groengele kleur. Chloor vormt met sommige chemicaliën explosieve verbindingen, maar chloor is op zich niet ontvlambaar.
Tijdens de Eerste Wereldoorlog werd het als wapen gebruikt om mensen te verstikken. Tegenwoordig wordt chloor gebruikt in pesticiden, rubber, oplosmiddelen en in zwemwater. Het wordt ook gebruikt bij de verwerking van afval. Houdt er rekening mee dat je dagelijkse chloorbleekmiddel, als het wordt gemengd met andere chemicaliën voor schoonmaken, kan veranderen in chloorgas. Wees voorzichtig als u het om welke reden dan ook gebruikt.
Chlorides worden ook gebruikt in de olie-industrie. Ze maken deel uit van het moddersysteem en ze worden daarom nauw gezet gemonitord. Als de hoeveelheid chloride in de modder toeneemt kan dit een signaal zijn dat er in zoutwaterformaties wordt geboord en die worden gekenmerkt door een hoge druk. De toename van chloride kan echter ook een signaal zijn dat de zanden waarin wordt geboord van slechte kwaliteit zijn.