Complexometrische titratie – principe, types, toepassingen, indicatoren en voorbeeld
Inhoudsopgave
Een complexometrische titratie is een soort volumetrische analyse waarbij de vorming van een gekleurd complex wordt gebruikt om het eindpunt van de titratie te bepalen. Het wordt voornamelijk gebruikt om metaalionen te kwantificeren door gebruik te maken van complexvormingsreacties.
Titrimetrie is de meest gebruikelijke kwantitatieve en volumetrische laboratoriumtechniek die wordt gebruikt om de onbekende concentratie van een opgeloste stof te bepalen door deze te vergelijken met de bekende concentratie van een oplossing in aanwezigheid van een indicator.
Bij het overwegen van doelen en processen zijn er verschillende soorten titraties te onderscheiden; zoals zuur-basetitraties, redox-titraties, neerslagtitraties en complexometrische titraties. Redoxtitraties en zuur-basetitraties zijn de meest gebruikte in de kwantitatieve chemische analyse.
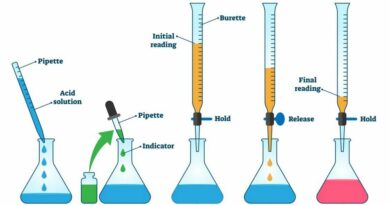
De gebruikelijke apparatuur voor een titratie bestaat uit een bekerglas, erlenmeyer, trechter, buret, pipet, wasfles, etc.
Wat is een complexometrische titratie?
Complexometrie wordt ook wel chelatometrie genoemd. Volumetrische titraties of analyses waarbij de eindpunten worden gespecificeerd door gekleurde verbindingen staan bekend als complexometrische titraties.
Bij complexometrische titraties wordt een indicator gebruikt die een duidelijke kleurverandering in de titratie kan veroorzaken, die het eindpunt of equivalentiepunt van de titratie aangeeft, dat afhankelijk is van de vorming van een complex tussen de analyt en de titrant. Het is erg handig voor het bepalen van de concentratie van een mengsel van metaalionen in de monsteroplossing.
De bepaling van de hardheid van water met behulp van EDTA met eriochroom zwart-T als indicator is een voorbeeld van een complexometrische titratie.
Principe van een complexometrische titratie
Wanneer de indicator eriochroom zwart-T zich bindt met metaalionen wordt het wijnrood, maar wanneer het vrij is van metaalionen blijft het blauw van kleur. Terwijl ethyleendiaminetetraazijnzuur (EDTA) kleurloos is, ongeacht of het al dan niet aan een metaalion is gekoppeld.

Omdat eriochroom zwart-T zicht bindt aan metaalionen, wordt het door toevoeging van een indicator aan het monster wijnrood van kleur. Eriochroom zwart-T is losjes gebonden met metaalionen terwijl EDTA sterk bindt met metaalionen. Daarom, wanneer alle metaalionen aan EDTA zijn gebonden, blijft de eriochroom zwart-T-indicator in de monsteroplossing vrij en lijkt de oplossing blauw.
Types van complexometrische titraties
Als chelerende titrant kan het ethyleendiaminetetraazijnzuur (EDTA) op verschillende manieren worden gebruikt. Daarom kunnen de titraties met EDA in verschillende typen worden uitgevoerd. Enkele staan hieronder beschreven.
Directe titratiemethode
De directe titratiemethode is vergelijkbaar met de zuur-basetitratie en is eenvoudig en handig. Bij deze methode wordt de standaard EDTA-oplossing met behulp van een buret geleidelijk toegevoegd aan de metaalionenoplossing totdat het gewenste eindpunt is bereikt.
Directe titraties worden gebruikt om koper, kwik, zink, barium, chroom, aluminium en lood, etc, te bepalen waarin de oplossing die het te bepalen metaalion bevat wordt gebufferd tot de vereiste Ph en direct wordt getitreerd met een standaard EDTA-oplossing.
Terugtitratiemethode
Een terugtitratie is een soort complexometrische titratie waarbij de analytconcentratie wordt bepaald door te reageren met een bekende overmaat reagens. Metaalionen die niet direct getitreerd kunnen worden met EDTA worden bepaald met behulp van de terugtitratiemethode.
Vervangende titratiemethode
De vervangende titratiemethode wordt gebruikt wanneer directe titratie of terugtitratie geen scherpe eindpunten oplevert. Het metaalion wordt bepaald door zink- of magnesiumionen uit een EDTA-complex te vervangen door een equivalent aantal metaalionen en vervolgens het vrijgekomen Zn- of Mg-ion te titreren met een standaard EDTA-oplossing.
Indirecte titratiemethode
De indirecte titratiemethode wordt vaak gebruikt wanneer normale titraties langzaam verlopen of het eindpunt moeilijk is te bepalen, evenals bij andere toepassingen zoals een zwak zuur-zwakke basereactie. Sommige anionen (bijvoorbeeld bariumionen) slaan neer als ze in contact komen met metaalionen en deze anionen reageren niet met EDTA. Daarom kan indirecte titratie met EDTA worden gebruikt om dit soort verbindingen te bepalen.
Toepassingen van complexometrische titraties
- De complexometrische titratie wordt gebruikt om de concentraties van metaalionen in monsteroplossingen te bepalen.
- Het wordt gebruikt voor de schatting van de hoeveelheid calcium die aanwezig is in voedingsmiddelen.
- Het wordt gebruikt om de totale hardheid van water te bepalen.
- Complexometrische titratie wordt vaak gebruikt in de farmaceutische industrie om de concentratie te bepalen van metaal in een farmaceutische doseringsvorm.
- Het wordt gebruikt in de analytische chemie om de zuiverheid te bepalen van stoffen.
- Complexometrische titraties worden gebruikt bij milieuanalyses om slechte metalen te bepalen.
- Cosmetische producten worden ook vaak geanalyseerd door middel van complexometrische titraties.
Welke indicator wordt gebruikt in complexometrische titraties
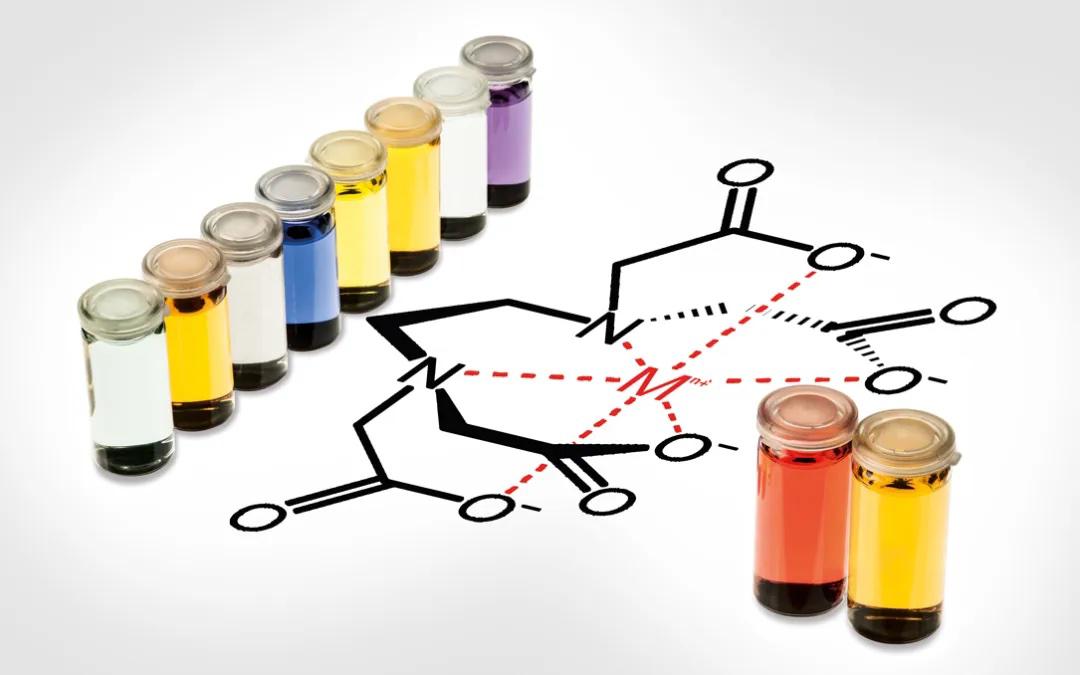
Complexometrische indicatoren zijn in water oplosbare moleculen die een belangrijke rol spelen bij de titratie om het eindpunt aan te geven. Deze indicatoren ondergaan een bepaalde kleurverandering in aanwezigheid van specifieke metaalionen. Veelgebruikte indicatoren bij complexometrische titraties zijn organische kleurstoffen, dit zijn organische moleculen die oplosbaar zijn in water. Wanneer het eindpunt is bereikt geeft een kleurverandering aan dat de indicator is verdrongen van de metaalkationen in de oplossing.
Voorbeelden van complexometrische indicatoren zijn eriochroom zwart T, calgamiet, arsenazo, xylenol-oranje, eriochroom rood B, snel sulfonzwart, calceïne, etc. Eriochroom zwart T, dat zowel als zuur/base-indicator als metaalionindicator fungeert, is de meest gebruikte indicator bij complexometrische titraties.
Methodes om het eindpunt in een complexometrische titratie te bepalen
Er zijn twee methodes om het eindpunt van een complexometrische titratie te bevestigen, namelijk de visuele methode en de instrumentele methode.
Visuele methode
De visuele methode is een van de meest populaire manieren om eindpunten te bepalen vanwege de voordelen: eenvoud, kosten efficiënt en precisie. Het bestaat uit metallochrome/PM-indicatoren, pH-indicatoren en redox-indicatoren.
Instrumentele methode
De instrumentele methode wordt ook gebruikt voor het bepalen van eindpunten van titraties. Instrumentele methodes berusten vaak op fotometrie of potentiometrie.
Eerste publicatie: 12 maart 2023