Volumetrische analyse – principes, types, procedures & toepassingen
Inhoudsopgave
Leer meer over het principe, de types, procedures en toepassingen van de volumetrische techniek die wordt gebruikt om de concentratie van een stof te bepalen met behulp van het bekende volume van een bekende stof.
Chemische analyse is een belangrijk onderdeel van de studie van verschillende materialen of stoffen. Het is grofweg ingedeeld in twee vormen: kwalitatieve analyse en kwantitatieve analyse. Kwalitatieve chemische analyse is een tak van de chemie die zich bezighoudt met de identificatie van elementen of groepering van elementen die aanwezig zijn in een monster.
Kwantitatieve analyse is elke techniek die wordt gebruikt om de concentratie van een stof in een monster te bepalen. Het is verder onderverdeeld in gravimetrische analyse en volumetrische analyse.
Titratie, oftewel titrimetrie, is een soort kwantitatieve analyse die wordt gebruikt om de hoeveelheid van een specifieke stof in een onbekend gegeven monster te bepalen. Omdat het meten van het volume het belangrijkste onderdeel van deze analyse is. Wordt het ook wel volumetrische analyse genoemd.
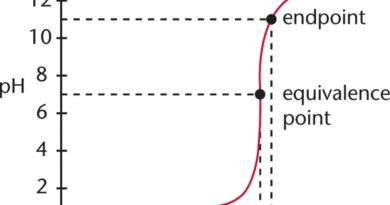
Daarbij wordt de titrant aan het analyt toegevoegd totdat een bepaald eindpunt of equivalentiepunt is bereikt. Het eindpunt van de reactie wordt geïdentificeerd met behulp van een indicator. De indicator veroorzaakt de kleur van de oplossing wanneer het eindpunt is bereikt.
Definitie van de volumetrische analyse: het proces van het titreren van een oplossing om aan de hand van het volume te bepalen hoeveel van een bepaalde substantie in de oplossing aanwezig is.
Wat is een volumetrische analyse
Een volumetrische analyse, ook bekend als een titratie, is een kwantitatieve chemische analysetechniek die in laboratoria wordt gebruikt om de concentratie van een analyt te bepalen door het meten van het volume van een tweede stof die wordt gecombineerd met de eerste in bekende proporties. Ook bekend als de titrimetrische analyse.
Met andere woorden, een volumetrische analyse oftewel een titratie verwijst naar het proces van het bepalen van het volume van een tweede stof die zich combineert met de eerste in bekende verhoudingen. Het wordt gebruikt in laboratoria waarmee we de concentratie van een analyt kunnen bepalen.
De titrant is een reagens dat een standaardoplossing produceerde met een specifiek volume en concentratie. De titrant reageert met een analyt-oplossing om de concentratie van de analyt te bepalen.
Geschiedenis van de volumetrische analyse
De Franse chemicus Jean-Baptiste-Andre Dumas heeft de eerste methode voor volumetrische analyse afgeleid en gevonden terwijl hij probeerde de hoeveelheid stikstof met andere elementen in organische verbindingen te kwantificeren.
Om de omzetting van de chemische stof in zuiver gas te verzekeren werd de stikstofverbinding in een oven verbrand en door de oven geleid in een stroom koolstofdioxide (CO2) die in een sterke alkalische oplossing werd geleid. De massa van het stikstof in het monster wordt berekend uitgaande van de bekende condities van druk en volume.
Voorbeelden van een volumetrische analyse
Volumetrie verwijst naar elke kwantitatieve analysemethode waarbij de hoeveelheid van een stof wordt bepaald door het volume te meten dat het inneemt, het volume van een tweede stof die in bekende verhoudingen met de eerste stof wordt gecombineerd.
Bijvoorbeeld een zuur-basetitratie, bereiding en standaardisatie van natriumhydroxide (NaOH)-oplossing.
Principe van een volumetrische analyse
- Onderstaand enkele grondbeginselen van de volumetrische analyse:
- De oplossing die moet worden onderzocht, moet een onbekend aantal chemicaliën bevatten.
- Om het eindpunt van de reactie aan te geven, reageert een chemische stof met een onbekende hoeveelheid met een stof met een onbekende concentratie in aanwezigheid van een indicator (bijvoorbeeld fenolftaleïne/methyloranje). Het eindpunt is het punt waarop een chemisch proces is voltooid.
- De titratieprocedure, die de volumes meet, wordt gebruikt om de reactie tussen de titrant en titrand te voltooien.
- De hoeveelheid reagens en oplossing wordt weergegeven door het volume en de concentratie van het reagens dat bij de titratie is gebruikt.
- De molfractie van de vergelijking bepaalt de hoeveelheid van een onbekende stof in een bepaald volume oplossing.
- Wanneer de reactie het eindpunt bereikt wordt het volume van de verbruikte reactant gemeten en gebruikt om de volumetrische analyse van de analyt (molariteit of normaliteit) te berekenen met behulp van de formule:
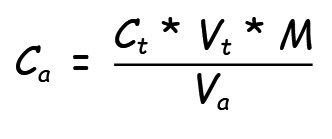
In deze formule is:
- Ca = Concentratie analyt
- Ct = concentratie titrant
- Vt = Volume titrant
- M = Molmassa
- Va = Volume analyt
Types volumetrische analyses
De volumetrische analyse kan worden onderverdeeld in drie types:
- Eenvoudige titratie
- Terugtitratie
- Dubbele titraties
Eenvoudige titratie
- Een eenvoudige titratie is een methode voor het bepalen van de concentratie van een onbekende oplossing gebruikmakende van een oplossing met een bekende concentratie. De eenvoudige titratie kan weer worden onderverdeeld in de volgende vier types:
- Zuur – basetitratie
- Redoxtitratie
- Precipitatie titratie
- Complexometrische titratie
Terugtitratie
Bij een terugtitratie wordt de concentratie van een analyt bepaald door de reactie met een overmaat van een bekend reagens terwijl bij een directe titratie de concentratie van een onbekende verbinding direct wordt onderzocht. Terugtitratie is ook bekend als indirecte titratie waarbij geen overmaat reagentia worden toegevoegd.
Dubbele titratie
Dit soort titraties wordt uitgevoerd om het procentuele gehalte van een zuur- of alkalimengsel te achterhalen. De titratiemethode volgens Gilson is ook bekend als de dubbele titratie. Ze bepaalt de concentratie van organometaalverbindingen in oplosmiddelen van koolwaterstoffen.
In de eerste stap wordt de baseconcentratie in de oplossing bepaald. De concentratie van het metaal-organische complex kan in de tweede trap worden berekend door de resterende hoeveelheid alkali te bepalen nadat de organometaalverbinding en het halogenide hebben gereageerd.
Volumetrische analyseprocedure
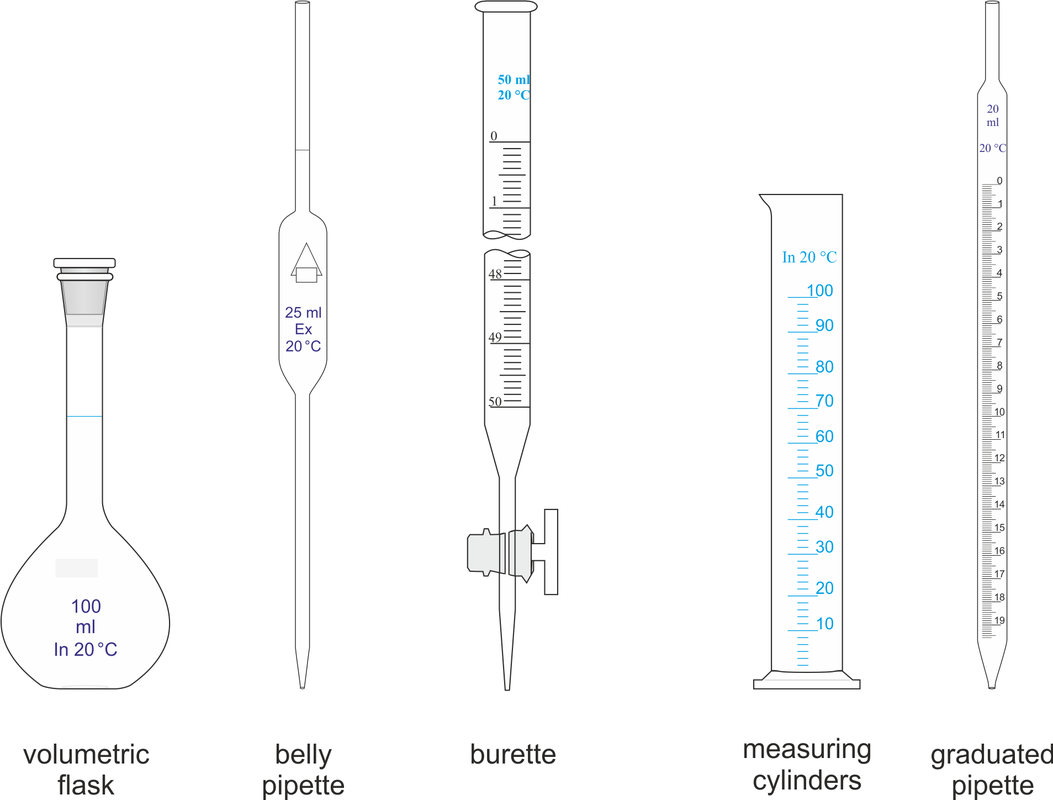
Gebruikelijke apparaten die nodig zijn om een volumetrische titratie uit te voeren zijn een buret, erlenmeyer, bekerglas, pipet, trechter, maatkolf, spoelfles, etc. hieronder staan de stappen die gebruikt kunnen worden bij een volumetrische analyse.
Al het glaswerk moet worden gereinigd en gedroogd volgens standaard laboratoriumprocedures.
Verwijder luchtbellen uit de buret en zet de aflezing op nul.
Door de chemicaliën nauwkeurig te wegen bereidt je nauwkeurig een standaardoplossing en een monster van het materiaal dat in de oplossing moet worden gemeten.
Een gewone titratie begint met het plaatsen van een erlenmeyer onder een buret, die de oplossing van analyt/monster en een paar druppels geschikte indicator (zoals methyloranje of fenolftaleïne) bevat.
Vervolgens wordt de titrant druppelsgewijs aan de analyt toegevoegd totdat een verandering in de kleur van de indicator wordt waargenomen, wat aangeeft dat het eindpunt van de titratie is bereikt. Dit geeft aan dat de aanwezige titrant gelijk is aan de aanwezige hoeveelheid analyt vanwege hun interactie.
Afhankelijk van het gewenste eindpunt kan een enkele druppel van de titrant een tijdelijke of permanente verandering in de kleur van de indicator veroorzaken.
Om nauwkeurige resultaten te verkrijgen wordt de titratie gewoonlijk drie keer herhaald en worden de aflezingen van de buret nauwkeurig genoteerd. Bereken het gemiddelde van het verkregen volume en bereken de normaliteit/molariteit van het monster.
Toepassingen van volumetrische analyses
Volumetrie is een van de fundamentele analytische technieken in de chemie en wordt toegepast voor kwantitatieve analyse in de biowetenschappen, farmacie, klinische chemie, cosmetische industrie, waterzuivering, afvalwaterbeheer, voedingsmiddelenindustrie, wijn, etc.
Eerste publicatie: 11 maart 2023