Voor- en nadelen van zuur – base titraties
Een zuur – base titratie is een kwantitatieve chemische analysemethode voor het schatten van de concentratie van een zuur of base. Het heeft verschillende voordelen en enkele nadelen. We bespreken ze in dit artikel.

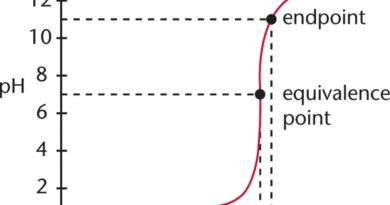
Titratie is een kwantitatieve laboratoriumtechniek die wordt gebruikt voor de bepaling van de analytconcentratie. Hierbij wordt de titrant vanuit een buret toegevoegd totdat de reactie voorbij is. Ook wordt er een indicator toegevoegd om het eindpunt of equivalentiepunt van de reactie weer te geven. Zuur – base, redox, neerslag en complexometrische titratie zijn soorten titraties die worden gebruikt voor verschillende soorten opgeloste stoffen.
Een zuur – basetitratie is een methode om de onbekende concentratie van zuur of base van een monsteroplossing te schatten door deze te neutraliseren met een bekende concentratie van zuur of base. De drie theorieën die voor titraties worden gebruikt zijn het Arrhenius-concept van zuur en base, het Bronstedt-Lowry-concept en het Lewis-concept. Op basis van het type reactie dat erbij betrokken is, worden zuur – basetitraties ingedeeld in vier typen: sterk zuur – sterke base, zwak zuur – sterke base, sterk zuur – zwakke base, zwak zuur – zwakke base. Enkele voorbeelden van indicatoren die bij titraties worden gebruikt zijn fenolftaleïne, methylrood, methyloranje, methylgeel, malachietgroen, fenolrood, thymolblauw, etc.
Voordelen van zuur – basetitraties
- Het grote voordeel van zuur – basetitraties is dat er geen speciale of dure chemicaliën nodig zijn. Je hebt reguliere chemicaliën zoals natriumhydroxide (NaOH), kaliumhydroxide (KOH), zoutzuur (HCl), zwavelzuur (H2SO4), azijnzuur (CH3COOH), mierenzuur (CH2O2), NH3, methylamine, etc. voor nodig.
- Je hebt er geen geavanceerde instrumenten voor nodig. Een buret en een erlenmeyer, beker, pipet, trechter, spoelfles en spatel zijn veel gebruikte middelen.
- Methodes voor zuur – base titraties zijn over het algemeen robuust.
- Vergeleken met andere methodes is het een kostenefficiënte methodiek.
- Het vereist geen speciale expertise, de bedieningsprocedures zijn relatief eenvoudig.
- De analyse koert niet veel tijd, het resultaat is snel beschikbaar.
- Er zijn verschillende soorten titraties beschikbaar voor verschillende soorten monsters (analyten).
Nadelen van zuur-base titraties
- Het grote nadeel van zuur – base titraties is dat de zuren en basen alleen worden gedefinieerd als waterige oplossingen en niet als stoffen.
- De theorie kan geen basische verbindingen verklaren die geen hydroxide-ion bevatten.
- Verschillende soorten titraties kunnen alleen binnen een bepaald pH-bereik en niet voor het hele pH-bereik.
- Het is een destructief proces dat vaak grote hoeveelheden chemicaliën verbruikt die worden geanalyseerd.
- Het grote nadeel van titraties is dat de reactie in een vloeibare fase moet plaatsvinden; het is niet geschikt voor vaste stoffen of opgeloste stoffen die oplosbaarheidsproblemen hebben.
- Net als bij andere titratiemethodes resulteert dit ook in een grote hoeveelheid chemisch afval dat moet worden afgevoerd.
- Het heeft een beperkte nauwkeurigheid en de precieze herhaalbaarheid is afhankelijk van de gebruiker; het kan moeilijk zijn om hetzelfde eindpunt te bepalen.
- Aangezien het een open systeem is kunnen temperatuur, luchtvochtigheid en sommige omgevingsfactoren de resultaten beïnvloeden.
Eerste publicatie: 11 maart 2023