Aluminium
Inhoudsopgave
Wat is Aluminum?
Aluminium heeft atoomnummer 13. Het is een zilverwit element dat lid is van de boorgroep van elementen. Na zuurstof en silicium is aluminium het meest voorkomende element op Aarde en het element dat het meeste voorkomt in de korst van de Aarde. Ongeveer 8% van de aardkorst bestaat uit aluminium. Aluminium is een heel reactief element dat met heel veel chemicaliën, elementen en verbindingen reageert en het komt niet in zuivere vorm voor in de natuur. Echter, er zijn meer dan 270 verschillende mineralen bekend waar aluminium in voorkomt. Het heeft een lage dichtheid en het is niet corrosief. Aluminium wordt om die eigenschappen veel in de vliegtuigindustrie toegepast. De meest bruikbare verbindingen zijn oxides en sulfaten.
| Symbool | Al |
| Volledige naam | Aluminium |
| Atoomnummer | 13 |
| Atoommassa (g.mol-1 ) | 26,9815 |
| Groep | post-transitiemetalen |
| Elektronegativiteit (Pauling) | 1,5 |
| Dichtheid (g.cm-3 bij 20 °C) | 2,7 |
| Smeltpunt (°C) | 660,4 |
| Kookpunt (°C) | 2467 |
| Vanderwaalstraal (nm) | 0,143 |
| Ionstraal (nm) | 0,05 |
| Isotopen | 17 waarvan 16 kunstmatig |
| Elektronenschilconfiguratie | 2, 8, 3 |
| Elektronenconfiguratie | [Ne]3s23p1 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 557,4 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1816,1 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 2744,1 |
| Standaard potentiaal (V) | -1,67 |
| Ontdekt door | Hans Christian Oersted in 1825 |
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 13 | Aluminium | 27 Al | 26,981538 | 100 |
Radioisotopen
| Symbool | Atoommassa (u) | Halfwaardetijd |
| 21 Al | 21,02804 | < 35 ns |
| 22 Al | 22,01952 | 59 ms |
| 23 Al | 23,007267 | 470 ms |
| 24 Al | 23,9999389 | 2,053 s |
| 25 Al | 24,9904281 | 7,183 s |
| 26 Al | 25,98689169 | 7,17 * 105 jaar |
| 27 Al | 26,98153863 | stabiel |
| 28 Al | 27,98191031 | 2,2414 min |
| 29 Al | 28,9804450 | 6,56 min |
| 30 Al | 29,982960 | 3,60 s |
| 31 Al | 30,983947 | 644 ms |
| 32 Al | 31,98812 | 31,7 ms |
| 33 Al | 32,99084 | 41,7 ms |
| 34 Al | 33,99685 | 56,3 |
| 35 Al | 34,9998638,6 | 38,6 |
| 36 Al | 36,00621 | 90 ms |
| 37 Al | 37,01068 | 10,7 ms |
| 38 Al | 38,01723 | 7,6 ms |
| 39 Al | 39,02297 | 7,6 ms |
| 40 Al | 40,03145 | 10 ms |
| 41 Al | 41,03833 | 2 ms |
| 42 Al | 42,04689 | 1 ms |
Bohr-Rutherford diagram
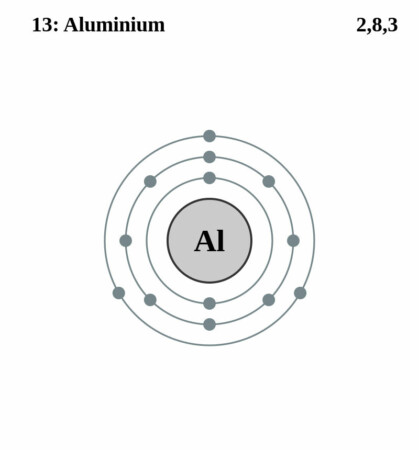
By Pumbaa (original work by Greg Robson) – Application: (generated by script), CC BY-SA 2.0 uk,
Spectra
Absorptiespectrum
Emissiespectrum
Oxides ontstaan als elementen in contact komen met zuurstof in de lucht, dit betekent dat ze zijn geoxideerd. De korst van de Aarde bestaat voor het overgrote deel uit oxides. Aan de andere kant zijn sulfaten zouten van zwavelzuur en ook die komen veel voor in de natuur. Ondanks dat aluminiumzouten voor voorkomen in de natuur worden ze niet door een levensvorm gebruikt.
Aluminium komt voor in verschillende verbindingen waaronder oxides en hydroxides, halides, nitride, carbide en gerelateerde metalen. Organische aluminiumverbindingen vallen ook in deze groep en worden algemeen in de chemische industrie gebruikt.
Door de verscheidenheid aan combinaties van eigenschappen van aluminium zijn de toepassingen ervan zeer divers. Het element wordt gebruikt in verschillende domeinen zoals handel, industrie, transport en meer. De toepassingen voor aluminium liggen niet altijd voor de hand. Aluminiumoxide wordt bijvoorbeeld gebruikt bij de productie van glas. Het element wordt vanwege zijn lage gewicht ook gebruikt in de transportindustrie. Door deze eigenschap hoeft er minder energie verbruikt te worden in het verplaatsen van voortuigen die van aluminium zijn gemaakt. Deze eigenschap komt ook zeer goed van pas bij de productie van vliegtuigen.
Aluminium is een zacht, licht en gemakkelijk te vervormen maar toch zeer duurzaam element. Soms is het oplosbaar in water maar niet in alcohol. De dichtheid van aluminium is ongeveer 1/3de van de dichtheid van staal. Het kan gemakkelijk worden verwerkt, gegoten en getrokken worden. Als aluminium in contact komt met lucht vormt zich aan het oppervlak een laagje aluminiumoxide. Dit zorgt er voor dat het oxidatieproces stopt. Aluminium roest dus niet.
Aluminium wordt vaak in zilverkleurige verven gebruikt want het heeft in poedervorm een reflecterend vermogen. Van alle metalen heeft aluminium in UV- en infrarood licht het hoogste reflecterend vermogen. In het zichtbare deel van het spectrum is aluminium derde na tin en zilver.
Aluminium is een warmtegeleider en het geleidt ook elektriciteit. Het warmte en elektriciteit geleidende vermogen van aluminium is 59% ten opzichte van koper. Aluminium kan ook als supergeleider gebruikt worden want het heeft een kritische temperatuur van 1,2 Kelvin.
Stabiel aluminium ontstaat uit de fusie van magnesium en waterstof. Dit vindt plaats in grote sterren of tijdens supernova-explosies. Het element is 100% recyclebaar en er gaan geen kwaliteiten verloren.
Tijdens het recyclen wordt het afval gesmolten. Dit kost slechts 5% van de energie die nodig is om aluminium uit erts te winnen. Nadeel is dat ongeveer 15% van het oorspronkelijke materiaal hierbij verloren gaat. Aluminium kan ook weer uit het ontstane afvalproduct worden gewonnen.
Wonderbaarlijk metaal
Aluminium ontstaat in sterren tijdens een fusiereactie waarbij magnesium een extra proton opneemt. Het wordt echter niet in pure vorm in de natuur gevonden. In de aardkorst komt aluminium het meest voor als een verbinding die aluin wordt genoemd (kaliumaluminiumsulfaat).
In 1825 was het de Deense chemicus Hans Christian Oersted die als eerste aluminium uit aluin wist te extraheren. Latere wetenschappers verfijnden het proces om aluminium uit aluin te halen maar ze waren niet in staat om de prijs tot een praktisch niveau te verlagen.
Aluminium werd decennia lang hoger gewaardeerd dan goud. Napoleon III, de eerste president van de Franse Tweede Republiek vanaf 1848, bediende trots zijn meest geëerde gasten met aluminium borden en bestek. Napoleon III had, naar verluidt, ook een aluminium rammelaar laten maken voor zijn zoon.
Uiteindelijk waren het Paul Heroult en Charles Hall die in 1886, onafhankelijk van elkaar, een proces ontwikkelden waarbij aluminiumoxide wordt gesmolten in cryoliet (natriumaluminiumfluoride) en wordt blootgesteld aan een elektrische stroom. Dit Hall-Heroult proces wordt tegenwoordig nog steeds gebruikt om aluminium te produceren naast het Bayer-proces dat aluminium extraheert uit bauxiet.
Het enige stabiele isotoop van aluminium is 27 Al. De meeste isotopen hebben een halfwaardetijd van slechts enkele milliseconden. Het langstlevende radioactieve isotoop is 26Al. Dit isotoop heeft een halfwaardetijd van 730.000 jaar. Dit isotoop is aangetroffen in stervormingsgebieden in ons sterrenstelsel. In die studie gebruikten wetenschappers van de NASA detecteerbare uitbarstingen van 26 Al om supernova’s en andere sterexplosies te lokaliseren. Met behulp van deze 26Al vingerafdrukken schatten wetenschappers dat er gemiddeld iedere 50 jaar een supernova voorkomt in ons sterrenstelsel en dat er jaarlijks 7 nieuwe sterren ontstaan.