Boor
Inhoudsopgave
Beschrijving
Boor (symbool B, atoomnummer 5) is een chemisch element en een metalloïde. Boor wordt niet gemaakt tijdens de nucleosynthese in sterren en daarom komt het maar in geringe hoeveelheden voor in de korst van de Aarde en in ons zonnestelsel. Omdat boraten goed oplossen in water, boor komt voor in boraat mineralen, komt het geconcentreerd voor op Aarde. Boraat mineralen worden gewonnen door het verdampen van ertsen waaronder borax (natriumtetraboraat, (Na2 B4 O7.10H2 O) en kerniet (Na2 B4 O6 (OH)2.3H2 O).
Gegevens Boor
| Symbool | B |
| Volledige naam | Borium – Boor |
| Atoomnummer | 5 |
| Atoommassa (g.mol-1 ) | 10,811 |
| Groep | Metalloïden |
| Elektronegativiteit (Pauling) | 2,04 |
| Dichtheid (g.cm-3 bij 20°C) | 2,3 |
| Smeltpunt (°C) | 2300 |
| Kookpunt (°C) | 2550 |
| Vanderwaalsstraal (nm) | 0,098 |
| Ionstraal (nm) | 0,027 |
| Isotopen | — |
| Elektronenconfiguratie | [He]2s2 2p1 |
| Eerste ionisatiepotentiaal (kJ.mol-1) | 800,5 |
| Tweede ionisatiepotentiaal (kJ.mol-1) | 2426,5 |
| Derde ionisatiepotentiaal (kJ.mol-1) | 3658,7 |
| Ontdekt door | Humphry Davy en Gay-Lussac in 1808 |
De chemisch zuivere vorm van boor komt van nature niet op Aarde voor. Zuiver boor is niet gemakkelijk te produceren omdat het verschillende vuurvaste materialen vormt samen met andere elementen (bijvoorbeeld koolstof).
Boor is ontdekt door de Franse chemici Louis-Jacques Thénard en Joseph-Louis Gay-Lussac en onafhankelijk van deze twee door de Engelse chemicus Sir Humphry Davis. De drie isoleerden het element door kalium en boorzuur te combineren.
Tegenwoordig wordt zuiver boor geproduceerd door borax te verhitten met koolstof.
Bohr-Rutherford diagram
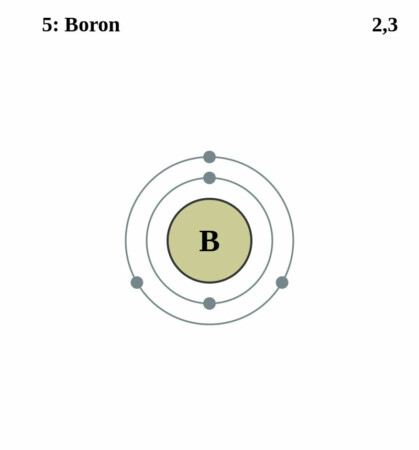
By Pumbaa (original work by Greg Robson) – CC BY-SA 2.0 uk,
Isotopen
| Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|
| Boor | 10 B | 10,012937 | 19,9 |
| 11 B | 11,009305 | 80,1 |
Radioactieve isotopen
| Symbool | Atoommassa (u) | Halfwaardetijd |
|---|---|---|
| 6 B | 6,04681 | onbekend |
| 7 B | 7,029918 | 570 * 10-24 s |
| 8 B | 8,024607 | 770 ms |
| 9 B | 9,013329 | 800 * 10-21 s |
| 12 B | 12,014352 | 20,20 ms |
| 13 B | 13,017780 | 17,33 ms |
| 14 B | 14,025404 | 12,5 ms |
| 15 B | 15,031103 | 9,97 ms |
| 16 B | 16,039809 | > 4,6 * 10-21 s |
| 17 B | 17,046990 | 5,08 ms |
| 18 B | 18,05617 | < 26 ns |
| 19 B | 19,06373 | 2,92 ms |
Spectra
Absorptiespectrum
Emissiespectrum
Toepassingen
Er zijn verschillende boorhoudende materialen die commercieel belangrijk zijn. Natriumboraat. pentahydraat is een van de belangrijkste. Om natriumperboraat, bleek en isolatie voor glasvezel te maken zijn er grote hoeveelheden natriumboraat.pentahydraat nodig. Ook boorzuur is een belangrijke stof. Het wordt gebruikt bij de productie van cellulose isolatie en textiel glasvezel. Natriumboraat.decahydraat (Borax) wordt gebruikt als ontsmettingsmiddel en voor de productie van wasmiddelen. Andere boorhoudende stoffen worden gebruikt om er metaal mee te bedekken en om er emaille mee te maken. Ook wordt het gebruikt voor de productie van borosilicaatglas en als een potentieel medicijn om gewrichtsontstekingen mee te behandelen. Boorfilamenten zijn lichte en zeer sterke materialen die voornamelijk worden gebruikt als onderdeel van composietmaterialen voor lucht- en ruimtevaartstructuren en voor de productie van sport- en consumptiegoederen zoals vishengels en golfclubs. Opdampen van het element op een wolfraamdraad kan worden gebruikt om de vezels te produceren.
Natriumperboraat wordt gebruikt als bron van actieve zuurstof in reinigingsmiddelen, wasmiddelen en bleekmiddelen. Boorzuur heeft ook een commercieel belang en wordt gebruikt als insecticide, vooral tegen kakkerlakken, vlooien en mieren. De chemische stof is ook een doteermiddel voor germanium, silicium, siliciumcarbide en andere halfgeleiders. Atomaire diffusie is de methode die wordt gebruikt om het element in halfgeleiders te introduceren, uitgevoerd bij hoge temperaturen. Gasvormige, vloeibare of vaste boorbronnen kunnen in het proces worden gebruikt. In fakkels en pyrotechniek produceert boor een groene kleur, en het is gebruikt als een ontstekingsbron in sommige raketten.
Een isotoop die in de natuur voorkomt, borium-10 absorbeert neutronen en wordt gebruikt als neutronendetector, als stralingsschild en in kernreactoren voor controlestaven. Chemisch gezien heeft boor meer overeenkomsten met silicium dan met thallium, indium en aluminium.
Boor heeft een zwarte kleur en het is semi-metallisch. Kristallijn boor is chemisch inert. Superharde boorverbindingen zijn onder andere boornitride, heterodiamant (BCN) en rheniumdiboride, dat een zeshoekig gelaagde structuur heeft. Boor heeft 14 isotopen waarvan er twee in de natuur voorkomen. Boor-10 oftewel verrijkt boor wordt gebruikt in de boorneutronenvangsttherapie en in de stralingsafscherming.