Moscovium
Inhoudsopgave
Moscovium is een radioactief, synthetisch element. Het wordt als een metaal geclassificeerd en men denkt dat het bij kamertemperatuur een vaste stof is. Het vervalt heel snel in andere elementen waaronder nihonium. Het element werd voorheen aangeduid als ununpentium, dit staat voor een-een-vijf in het Latijn. In november 2016 kreeg het van de International Union of Pure and Applied Chemistry (IUPAC) de officiële naam Moscovium. De IUPAC gaf ook de elementen 113 (Nihonium, Nh), 117 (Tennessine, Ts) en 118 (Oganesson, Og) hun officiële naam.
De namen voor de elementen 115 en 117 werden voor hun ontdekkers van het Joint Institute for Nuclear Research in Dubna, Rusland; het Oak Ridge National Laboratory in Tennessee; de Vanderbilt University in Tennessee en het Lawrence Livermore National Laboratory in California voorgesteld. Beide elementen, moscovium en tennessine, verwijzen naar de gebieden waar de experimenten die leidden tot hun ontdekking zijn uitgevoerd.
Chemische gegevens
| Symbool | Moscovium |
| Volledige naam | Mc |
| Atoomnummer | 115 |
| Atoommassa (g.mol-1 ) | 295 |
| Groep | post-transitie metaal |
| Elektronegativiteit (Pauling) | — |
| Dichtheid (g.cm-3 bij 20 °C) | 13,5 (berekend) |
| Smeltpunt (°C) | 400 (berekend) |
| Kookpunt (°C) | 1100 (berekend) |
| Vanderwaalsstraal (nm) | — |
| Ionstraal | — |
| Isotopen | — |
| Elektronenschil | [Rn]5f146d107s27p3 |
| Elektronen per schil | 2, 8, 18, 32, 32, 18, 5 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 538,3 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1760 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 2650 |
| Standaard potentiaal (V) | — |
| Ontdekt door: | 2003 door Joint Institute of Nuclear Research, Dubna, Rusland |
Ontdekking
Moscovium werd in 2003 ontdekt en op 2 februari 2004 officieel aangekondigd. Het werd gemaakt door wetenschappers van het Joint Institute for Nuclear Research in Dubna, Rusland en wetenschappers van het Lawrence Livermore National Laboratory in de Verenigde Staten.
Eigenschappen van Moscovium
Er zijn 4 isotopen met een bekende halfwaardetijd bekend. Het meest stabiele isotoop is 289 Mc dat een halfwaardetijd van ongeveer 330 milliseconden heeft.
De atoommassa van door mensen gemaakte transuranium elementen is gebaseerd op het langstlevende isotoop. Deze atoommassa’s zijn altijd onder voorbehoud want er kan een nieuw isotoop met een langere halfwaardetijd worden gevonden.
Isotopen
| Symbool | Atoommassa (u) | Halfwaardetijd |
|---|---|---|
| 287 Mc | 287,19070 | 37 ms |
| 288 Mc | 288,19274 | 164 ms |
| 289 Mc | 289,19363 | 330 ms |
| 290 Mc | 290,19598 | 650 ms |
Bohr-Rutherford diagram
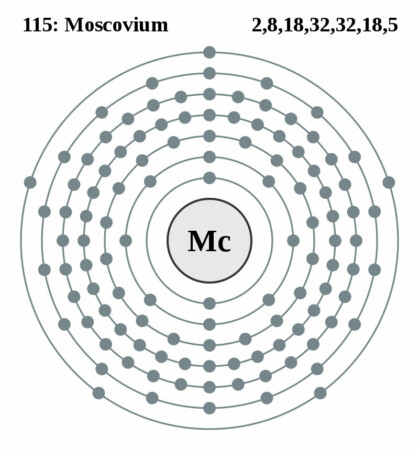
By Pumbaa (original work by Greg Robson), CC BY-SA 2.0 uk,