Holmium
Inhoudsopgave
Wat is Holmium?
Holmium heeft atoomnummer 67 en symbool Ho. Het behoort tot de zeldzame aardmetalen en de lanthaniden. Holmium is in 1878 ontdekt toen het als oxide werd gewonnen uit erts. Holmium is vernoemd naar de Zweedse hoofdstad Stockholm. Het element is ontdekt door de Zweedse chemicus Per Theodor Cleve en hij gebruikte dezelfde extractiemethode als Mosander gebruikte toen hij terbium, erbium en lanthaan ontdekte. Cleve zocht naar verontreinigingen in oxides en hij begon met erbia, het oxide van erbium. Na het verwijderen van verontreinigingen ontstonden er twee materialen. Eentje had een groene kleur en het andere was bruin. Cleve noemde het groene materiaal thulia en het bruine materiaal holmia. Thulia is thuliumoxide en holmia is holmiumoxide. Het absorptiespectrum van holmium was al eerder waargenomen door de Zwitserse chemici Delafontaine en Soret.
Gegevens
| Symbool | Ho |
| Volledige naam | Holmium |
| Atoomnummer | 67 |
| Atoommassa (g.mol-1 ) | 164,93 |
| Groep | Lanthaniden |
| Elektronegativiteit (Pauling) | 1,23 |
| Dichtheid (g.cm-3 bij 20 °C) | 8,8 |
| Smeltpunt (°C) | 1474 |
| Kookpunt (°C) | 2695 |
| Vanderwaalstraal (nm) | — |
| Ionstraal (nm) | — |
| Isotopen | 1 |
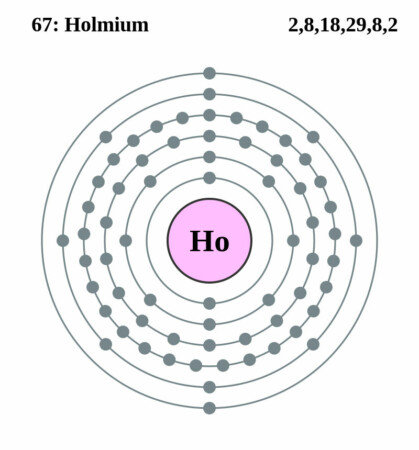
| Elektronenconfiguratie | [Xe]4f116s2 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 580 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1136,5 |
| Derde ionisatie potentiaal (kJ.mol-1 ) | 2203,74 |
| Standaard potentiaal (V) | -2,32 |
| Ontdekt door | Per Teodor Cleve in 1878 |
Bohr-Rutherford diagram
Holmium heeft een zilverwitte kleur, het is redelijk buigzaam en zacht. Omdat Holmium erg reactief is komt het niet in zuivere vorm in de natuur voor. Bij kamertemperatuur en onder vochtvrije omstandigheden is het echter stabiel. In contact met water treedt er snel oxidatie op en als holmium wordt verhit dan brandt het in de lucht. Bij hogere temperaturen en vochtige lucht oxideert holmium tot het witgele holmiumoxide. Afhankelijk van het soort licht dat op Holmium valt verandert het van kleur. In daglicht heeft holmium een gelige kleur en in trichromatisch licht lijkt het met een oranjerode kleur op erbiumoxide.
Holmium wordt vaak aangetroffen in de samenstelling van mineralen als gadoliniet en monaziet. In de natuur en onder laboratoriumomstandigheden bevatten holmiumverbindingen Ho(III)-ionen. Er is maar 1 stabiel isotoop van Holmium bekend: 165Ho. Er zijn diverse radioactieve isotopen van holmium. Van deze radioactieve isotopen is 163Holmium met een halfwaardetijd van 4570 jaar het meest stabiel.
Holmium is het krachtigste magnetische element. Holmium wordt daarom wel gebruikt om de polen van sterke statische magneten mee te maken. Omdat holmium een goede neutronenvanger is wordt het ook gebruikt in controlestaven van kernreactoren. Holmiumoxide wordt wel gebruikt om glas geel te kleuren. Het element wordt ook gebruikt in solid-state lasers die worden toegepast in de tandheelkunde en andere medische applicaties. Een Holmium-laser is veilig voor de ogen.
Holmium wordt gebruikt om glas en kubisch zirkonium rood en geel te kleuren. Glas dat holmiumoxide bevat vertoont scherpe optische absorptiepieken tussen een golflengte van 200 en 900 nm. Het radioactieve 166Holmium heeft een grote halfwaardetijd en wordt gebruikt voor de kalibratie van gammastralen spectrometers.
Ofschoon Holmium tot de zeldzame aardmetalen behoort komt het 20 maal meer voor dan zilver. Het komt niet in vrije vorm voor in de natuur. Jaarlijks wordt er ongeveer 10 ton Holmium gewonnen. Het wordt voornamelijk gevonden in India, Brazilië, China, Australië, de Verenigde Staten en Sri Lanka.
Holmium heeft geen biologische functie en het is een van de minst voorkomende elementen in ons lichaam. Ofschoon Holmium niet toxisch is stimuleert het wel het menselijke metabolisme. Holmium vormt geen gevaar voor het milieu, planten en dieren.
Isotopen
| Nummer | Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|---|
| 67 | Holmium | 165 Ho | 164,930319 | 100 |
Radioisotopen
| Nuclide | Isotopische massa (u) | Halfwaardetijd |
|---|---|---|
| 140Ho | 139,96854 | 6 ms |
| 141Ho | 140,96310 | 4,1 ms |
| 142Ho | 141,95977 | 400 ms |
| 143Ho | 142,95461 | 300 ms |
| 144Ho | 143,95148 | 0,7 s |
| 145Ho | 144,94720 | 2,4 s |
| 146Ho | 145,94464 | 3,6 s |
| 147Ho | 146,94006 | 5,8 s |
| 148Ho | 147,93772 | 2,2 s |
| 149Ho | 148,93377 | 21,1 s |
| 150Ho | 149,93349 | 76,8 s |
| 151Ho | 150,93168 | 35,2 s |
| 152Ho | 151,93171 | 161,8 s |
| 153Ho | 152,93019 | 2,01 min |
| 154Ho | 153,93060 | 11,76 min |
| 155Ho | 154,92910 | 48 min |
| 156Ho | 155,92984 | 56 min |
| 157Ho | 156,92825 | 12,6 min |
| 158Ho | 157,92894 | 11,3 min |
| 159Ho | 158,92771 | 33,05 min |
| 160Ho | 159,92872 | 25,6 min |
| 161Ho | 160,92785 | 2,48 uur |
| 162Ho | 161,92909 | 15,0 min |
| 163Ho | 162,92873 | 4570 jaar |
| 164Ho | 163,93023 | 29 min |
| 165Ho | 164,93032 | stabiel |
| 166Ho | 165,93228 | 26,83 uur |
| 167Ho | 166,93313 | 3,003 uur |
| 168Ho | 167,93552 | 2,99 min |
| 169Ho | 168,93687 | 4,72 min |
| 170Ho | 169,93962 | 2,76 min |
| 171Ho | 170,94147 | 53 s |
| 172Ho | 171,94482 | 25 s |
| 173Ho | 172,94729 | 10 s |
| 174Ho | 173,95115 | 8 s |
| 175Ho | 174,95405 | 5 s |