Thorium
Inhoudsopgave
Naamgeving
Thorium is vernoemd naar de Noorse god van de donder. Het is een zilverkleurig, glanzend en radioactief element dat uranium als brandstof voor kernreactoren kan vervangen.
Chemische gegevens
| Symbool | Th |
| Volledige naam | Thorium |
| Atoomnummer | 90 |
| Atoommassa (g.mol-1 ) | 232,0 |
| Groep | actiniden |
| Elektronegativiteit (Pauling) | 1,3 |
| Dichtheid (g.cm-3 bij 20 °C) | 11,7 |
| Smeltpunt (°C) | 1750 |
| Kookpunt (°C) | 4788 |
| Vanderwaalsstraal (nm) | 0,182 |
| Ionstraal (nm) | 0,110 (+4) |
| Isotopen | 1 stabiel, 8 radioactief |
| Elektronenschil | [Rn]6d27s2 |
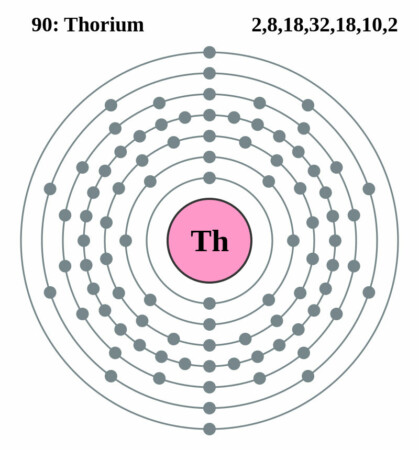
| Elektronen per schil | 2, 8, 18, 32, 18, 10, 2 |
| Eerste ionisatiepotentiaal (kJ.mol-1 ) | 587 |
| Tweede ionisatiepotentiaal (kJ.mol-1 ) | 1110 |
| Derde ionisatiepotentiaal (kJ.mol-1 ) | 1930 |
| Standaard potentiaal (V) | — |
| Ontdekt door: | 1829 door Jöns Jakob Berzelius |
Isotopen
| Naam | Symbool | Atoommassa (u) | Abundantie (%) |
|---|---|---|---|
| Th | 230Th | 230,0331341 | 0,02 |
| 232Th | 232,0380558 | 99,98 |
Radioisotopen
| Nuclide | Atoommassa (u) | Halfwaardetijd |
|---|---|---|
| 209Th | 209,01772 | 7 ms |
| 210Th | 210,015075 | 17 ms |
| 211Th | 211,01493 | 48 ms |
| 212Th | 212,01298 | 36 ms |
| 213Th | 213,01301 | 140 ms |
| 214Th | 214,011500 | 100 ms |
| 215Th | 215,011730 | 1,2 s |
| 216Th | 216,011062 | 26,8 ms |
| 218Th | 218,013284 | 109 ns |
| 221Th | 221,018184 | 1,73 ms |
| 222Th | 222,018468 | 2,237 ms |
| 223Th | 223,020811 | 0,60 s |
| 224Th | 224,021467 | 1,05 s |
| 225Th | 225,023951 | 8,72 min |
| 226Th | 226,024903 | 30,57 min |
| 227Th | 227,0277041 | 18,68 dagen |
| 228Th | 228,0287411 | 1,9116 jaar |
| 229Th | 229,031762 | 7,34 × 103 jaar |
| 230Th | 230,0331338 | 7,538 × 104 jaar |
| 231Th | 231,0363043 | 25,52 uur |
| 232Th | 232,0380553 | 1,405 * 1010 jaar |
| 233Th | 233,0415818 | 21,83 min |
| 234Th | 234,043601 | 24,10 d |
| 235Th | 235,04751 | 7,2 min |
| 236Th | 236,04987 | 37,5 min |
| 237Th | 237,05389 | 4,8 min |
| 238Th | 238,0565 | 9,4 min |
Geschiedenis
In 1815 dacht de Zweedse chemicus Jöns Jakob Berzelius dat hij een nieuw aards element had gevonden. Hij vernoemde het naar Thor, de Noorse god van de oorlog. In 1824 kwam men er achter dat Berzelius eigenlijk het mineraal yttriumfosfaat had gevonden.
In 1828 kreeg Berzelius een monster van een zwart mineraal dat op Løvø was gevonden. Løvø is een eiland voor de Noorse kust. Dit mineraal bevatte ongeveer 60% van een onbekend element en dit element kreeg de naam thorium. Het mineraal kreeg de naam thoriet. Het element bevatte ook veel bekende elementen als ijzer, mangaan, lood, tin en uranium.
Berzelius isoleerde thorium door thoriumoxide te mengen met koolstof om zo thoriumchloride te verkrijgen. Dit liet hij reageren met kalium om er kaliumchloride en thorium uit te verkrijgen.
In 1898 ontdekten Gerhard Schmidt en Marie Curie onafhankelijk van elkaar en met enkele maanden tussentijd dat thorium radioactief is.
De halfwaardetijd van thorium werd ontdekt door Ernest Rutherford en Frederick Soddy. Hun werk leverde een belangrijke bijdrage aan de kennis over andere radioactieve elementen.
In 1925 slaagden de Nederlandse chemici Anton Eduard van Arkel en Jan Hendrik de Boer er in om zeer zuiver metallisch thorium te produceren.
Bohr-Rutherford diagram
Weetjes
- In vloeibare vorm heeft thorium het grootste temperatuurbereik van alle bekende elementen. Tussen smeltpunt en kookpunt bijna 3000 °C.
- Van alle bekende oxides heeft thoriumoxide het hoogste smeltpunt.
- Thorium komt net zo veel voor als lood en bijna drie keer zo veel als uranium.
- In de korst van de Aarde bevindt zich 6 ppm thorium. Het is daarmee het 41ste meest voorkomende element in de korst van de Aarde.
- Thorium wordt voornamelijk gewonnen in Australië, Canada, de Verenigde Staten en India.
- Sporen thorium zijn gevonden in gesteente, grond, water, planten en dieren.
- Hogere concentraties thorium worden aangetroffen in mineralen als thoriet, thorianiet, monaziet, allaniet en zirconium.
- Het meest stabiele isotoop is 232Th. Dit isotoop heeft een halfwaardetijd van 14 miljard jaar.
- Thorium wordt gemaakt in de kern van supernovae en dan tijdens explosies verspreid door het heelal.
- Sinds 1885 is thorium gebruikt in gasmantels maar vanwege zijn radioactiviteit is het vervangen door niet-radioactieve zeldzame aardmetalen.
- Thorium wordt ook gebruikt om magnesium te versterken, wolfraamdraad in elektrische apparatuur te coaten, de korrelgrootte van wolfraam te regelen in elektrische lampen, smeltkroezen voor hoge temperaturen, in glazen, in lenzen voor camera’s en wetenschappelijke instrumenten. Bovendien is thorium een bron voor kernenergie.
- Andere toepassingen voor thorium zijn onder meer hittebestendig keramiek, vliegtuigmotoren en in gloeilampen. Ook werd thorium, voordat de gevaren van radioactiviteit werden ontdekt, toegepast in tandpasta’s.
- Thorium en uranium zijn betrokken bij de verwarming van het binnenste van de Aarde.
- Teveel blootstelling aan thorium kan leiden tot longziektes, long- en alvleesklierkanker, genetische afwijkingen, leverziektes, botkanker en metaalvergiftiging.
Huidig onderzoek
Een groot deel van het huidige onderzoek is gericht op thorium als brandstof voor nucleaire reactoren. Thorium heeft diverse voordelen boven uranium:
- Er komt drie tot vier keer meer thorium dan uranium voor op Aarde
- Thorium is gemakkelijker te winnen dan uranium.
- Reactoren met vloeibare thoriumfluoride produceren veel minder afval dan reactoren die door uranium worden aangedreven.
- Een thoriumreactor werkt op atmosferische druk in plaats van de 150 tot 160 bar die nodig is bij een uraniumreactor.
- Thorium is minder radioactief dan uranium.
In de jaren ’50 werd in de Verenigde Staten gewerkt aan de ontwikkeling van thoriumreactoren ter ondersteuning van programma’s voor nucleaire vliegtuigen. Het programma stopte in 1961 ten gunste van andere technologieën. Dit werd gedaan omdat thoriumreactoren minder plutonium produceren als door uranium aangedreven reactoren. In die tijd was plutonium, evenals uranium vanwege de Koude Oorlog erg belangrijk.
Thorium zelf wordt niet gebruikt voor nucleaire brandstof maar het wordt gebruikt om het kunstmatige uraniumisotoop 233U te maken. 232Th absorbeert eerst een neutron waardoor 233Th ontstaat. Dit vervalt binnen 4 uur tot 233Pa. Dit proactinium-233 vervalt in ongeveer 10 maanden tot 233U. Uranium-233 wordt vervolgens als brandstof in kernreactoren gebruikt.
Spectra
Absorptiespectrum
Emissiespectrum
Laatste update: 2021-05-30