De chemie van honing

Honing is een vreemd goedje omdat het, in tegenstelling tot de meeste voedingsmiddelen, na verloop van tijd niet bederft. In feite was de oudste bekende honing, gevonden in een oud-Egyptisch graf en gedateerd op ongeveer 3000 jaar oud, vermoedelijk nog steeds perfect eetbaar. Wat geeft honing deze ongewone eigenschap?
Om deze vraag te kunnen beantwoorden moeten we begrijpen hoe honing door bijen wordt gemaakt. Honing is afkomstig van plantennectar, een mix van verschillende suikers, eiwitten en andere verbindingen in een waterige oplossing. Hoewel de samenstelling van nectar van plant tot plant verschilt en er vaak een reek chemische verbindingen aanwezig is, is sucrose meestal de dominante duiker. Dit is eigenlijk precies dezelfde suiker als in de keuken, de tafelsuiker. De verschillende concentraties van de verschillende componenten van nectar in de verschillende nectars is de reden dat er verschillende soorten honing zijn, afhankelijk van het type nectar dat de bijen voornamelijk verzamelen.
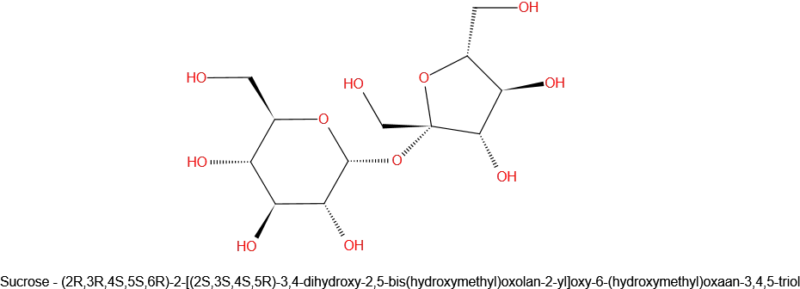
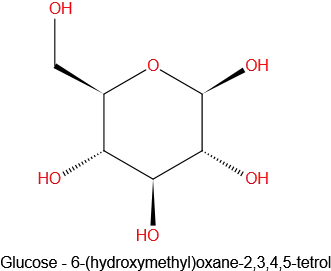
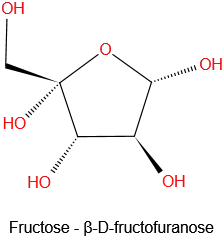
Bijen zijn de belangrijkste tussenstop tussen nectar en honing. Werkbijen verzamelen de nectar van bloemen en slaan deze op in hun honingmaag. Dit is een andere maag dan hun normale maag. Enzymen die door klieren worden uitgescheiden worden vervolgens gemengd met de nectar. Deze enzymen beginnen met de afbraak van de sucrose in de nectar tot eenvoudige suikers. Sucrose is wat we een disacharide noemen; het bestaat uit twee eenvoudige suikers, glucose en fructose. In de honingmaag van de bij worden de sucrosemoleculen geleidelijk door de enzymen gesplitst in glucose en fructose.
Glucose en fructose kunnen ook respectievelijk dextrose en levulose worden genoemd. Deze twee suikers zijn eigenlijk structurele isomeren, ze hebben dezelfde chemische formule. De namen “dextrose” en “levulose” verwijzen naar hun effect op vlak gepolariseerd licht. Vanwege het verschil in rangschikking van de atomen roteert dextrose vlak-gepolariseerd licht naar rechts terwijl levulose het naar links polariseert. De voorvoegsels “dextro-“ en “levulo-“ komen uit het Latijn voor respectievelijk rechts en links.
Zodra de werkbij terugkeert naar de korf zal hij de nectaroplossing uitbraken en deze doorgeven aan een van de huisbijen die in de korf blijven. De huisbij zal het proces voortzetten dat de werkbij is begonnen – gedurende maximaal 20 minuten zal hij de nectar uitbraken en opnieuw drinken, het blijven mengen met enzymen en het verder afbreken. Hoewel er nog wat sucrose achterblijft wordt het grootste deel afgebroken tot fructose en fructose.
Zodra een geschikte afbraak is bereikt deponeert de huisbij de nectar in de honingraat in de korf. Dan begint een andere belangrijke stap in het proces. Nectar kan tot 70% water bevatten en dit water moet worden verdampt om de consistentie van honing te produceren die we allemaal kennen. Dit bereiken de bijen door met hun vleugels de honingraat uit te waaien om zo een snelle verdamping van het water uit het nectarmengsel te stimuleren. Uiteindelijk zal het watergehalte van de oplossing dalen tot ongeveer 17%, veel minder dan het oorspronkelijke gehalte van de nectar. De omzetting van de waterige nectar naar stroperige honing duurt tussen de 1 en 3 dagen.
Het watergehalte van honing is een belangrijke factor waarom het niet bederft. Met 17% is het watergehalte veel lager dan dat van bacteriën of schimmels. Honing heeft ook een lage wateractiviteit; dit is een maat voor de hoeveelheid water in een stof die beschikbaar is om microbiële groei te ondersteunen. Wateractiviteit ligt op een schaal van 0 tot 1, waarbij de meeste schimmels en bacteriën niet kunnen groeien onder een wateractiviteit van 0,75. Honing heeft een wateractiviteit van 0,6. Dit, in combinatie met het feit dat het lage watergehalte bacteriën uitdroogt maakt het bestand tegen bederf.
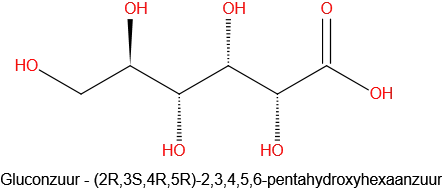
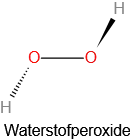
Een andere factor die ervoor zorgt dat honing niet bederft is de zuurgraad. De gemiddelde pH is ongeveer 4. Deze zuurgraad wordt veroorzaakt door een aantal zuren, waaronder mierenzuur en citroenzuur. Maar het dominante zuur is gluconzuur end at wordt geproduceerd door de werking van bijenenzymen op sommige glucosemoleculen in de honing. Dit versterkt de antibacteriële eigenschappen van de honing verder want veel bacteriën gedijen in neutrale in plaats van zure omstandigheden. Door de productie van gluconzuur ontstaat er ook waterstofperoxide en ook dit kan de groei van bacteriën remmen. De antibacteriële eigenschappen van honing zijn eigenlijk krachtig genoeg om te gebruiken als een geïmproviseerd wondverband.
|
|
Tot slot zou je kunnen opmerken dat honing na verloop van tijd de neiging heeft te kristalliseren en te stollen. Omdat het watergehalte van honing zo laag is, kan het worden beschouwd als een oververzadigde oplossing van verschillende suikers. Een oplossing wordt als verzadigd beschouwd als er zoveel mogelijk vaste stof in is opgelost. Na verloop van tijd zal glucose uit de oplossing neerslaan en vaste kristallen vormen. De honing is nog steeds prima te eten en dit is ook geen bederf. Om het terg te brengen naar zijn vloeibare vorm hoef je het alleen maar een paar minuten in warm water onder te dompelen.